PADRONIZAÇÃO DO NaOH E DETERMINAÇÃO DA ACIDEZ DO VINAGRE
MATERIAL UTILIZADO
PROCEDIMENTO
- Bureta de 50 mL.
- Garra de bureta.
- Pipeta de 20 ou 10 mL.
- Pêra de borracha.
- Suporte universal.
- Erlenmeyer de 250 mL.
- Becker de 100 mL.
- Funil.
- Pisseta.
- Provetas de 50 e 250 mL.
- Vinagre.
- Solução de hidróxido de sódio (NaOH) 0,1N.
- Solução de ácido clorídrico (HCl) 0,1N.
- Solução de fenolftaleína.

FIGURA 1 - Montagem do Experimento.
1 - Carregar a bureta de 50 mL com solução de NaOH 0,1 N.
2 - Calcular a massa de Ftalato ácido de potássio (padrão primário) necessária para neutralizar completamente 25 mL da solução de NaOH ~ 0,1 mol/L. Este volume corresponde a metade da capacidade da bureta, onde o erro é menor.
3 - Pesar a massa calculada três vezes, com precisão de ± 0,1 mg e transferir para erlenmeyers previamente enumerados. Não é necessário pesar exatamente os mesmos valores de massa, variações de ± 2,0 mg são aceitáveis.
4 - Dissolver os sólidos em 50 mL de água e adicionar 3 gotas de Fenolftaleína.
5 - Adicionar lentamente a solução da bureta ao erlenmeyer, segurando e agitando-o com a mão direita, com a mão esquerda controlar a torneira da bureta. Anotar o ponto final da titulação. Repetir a titulação para os outros dois erlenmeyers.

FIGURA 2 - Padronização do NaOH.
6 - Anotar os valores de acordo com a TABELA 1.
TABELA 1 - mpp, volume de NaOH e normalidade de
NaOH.
|
ERLENMEYER |
mpp (g) | VNaOH (mL) | NNaOH |
| 1 | |||
| 2 | |||
| 3 | |||
|
NNaOH = |
|||
7 - No caso de discrepância
significativa entre os valores de normalidade, repetir as titulações tantas
vezes quanto necessárias.
![]() DETERMINAÇÃO DA ACIDEZ DO VINAGRE.
DETERMINAÇÃO DA ACIDEZ DO VINAGRE.

FIGURA 3 - Montagem do Experimento de Determinação da
Densidade do Vinagre.
1 - Pesar com precisão de ± 1 mg 20 mL de vinagre e calcular a densidade do mesmo.
2 - Pipetar três vezes 2 mL de vinagre para três erlenmeyers de 250 mL.
3 - Adicionar cerca de 30 mL de água (medidos em proveta ) e de 5 gotas de fenolftaleína.
4 - Carregar a bureta com solução de NaOH padronizada.
5 - Adicionar ao erlenmeyer a solução de NaOH, gota a gota, com agitação constante, até a viragem do indicador. Observar e anotar a cor da viragem.
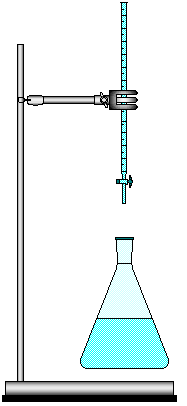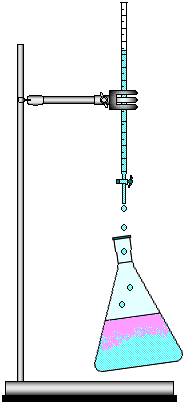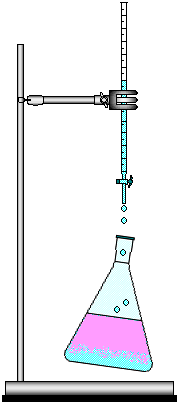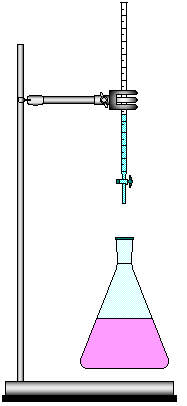
FIGURA 4 - Determinação da Acidez do Vinagre.
6 - Repetir a operação. Não admissíveis diferenças superiores a ± 0,1 mL entre as três titulações.
7 - Calcular a média entre os itens 5 e 6.