25/11/2009

|

|

|
Eziquiel Menta, Rosangela Menta Mello
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
O que o aluno poderá aprender com esta aula
Distinguir e identificar quando uma substância sofre o processo de Dissociação e o de Ionização, seguido de sua condutividade elétrica em solução aquosa.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
- Funções Inorgânicas:
* Classificação dos Ácidos
* Classificação das Bases
Estratégias e recursos da aula
Momento 01 -
Olá Professor !
Inicie a aula problematizando a seguinte questão com os alunos:

As substâncias que sofrem o processo de Dissociação e o de Ionização podem conduzir corrente elétrica na sua forma pura.


Fonte: http://www.pinhorepresentacoes.com.br/rajja_produtos.jpg acessado 18/11/09
Ácido Sulfúrico
Fonte: http://www.odisseia.univ-ab.pt/e-learning/workshop/ContMatema/ContMa3.gif acessado 18/11/09


Para que fique fácil o entendimento da nossa aula, faremos uma simples comparação de uma substância ácida e básica. Tomaremos como exemplo duas substâncias muito comum utilizadas no nosso dia-a-dia, que é o ácido clorídrico, componente principal de um material de limpeza chamado de "ácido muriático", e o hidróxido de sódio, encontrado na soda cáustica.
Vejam na tabela abaixo algumas características interessantes que essas substâncias possuem.
Covalente (substância molecular)| Caráter da ligação química principal | Iônica (substância iônica) | |
| Estado Físico (25ºC, 1atm) | Gás | Sólido |
| Condutividade elétrica da solução aquosa | Conduz | Conduz |
| Na presença de fenolftaleína | Solução Incolor | Solução Avermelhada |
| Ação sobre bicarbonato de sódio | Há efervescência | Não há efervescência |

A condutividade do hidróxido de sódio (NaOH) em solução aquosa
O hidróxido de sódio é uma substância iônica, ou seja, é um sólido que já existem cátions sódio (Na+) e ânions hidróxidos (OH-), agrupados com muita regularidade em um arranjo chamado retículo cristalino.
Quando em presença de água, o retículo cristalino se desmancha e os íons acabam ficando livres, a essa separação de íons chamamos de dissociação iônica que justifica a condutividade da solução. Essas soluções desse tipo são denominadas iônicas ou eletrolíticas.
Por que s solução aquosa de açúcar não conduz corrente elétrica.
Quando adicionamos açúcar à água, as moléculas se separam, mas não há formação de íons. A essa transformação denomina-se de dissociação molecular. A solução resultante é chamada de solução molecular ou não eletrolítica.
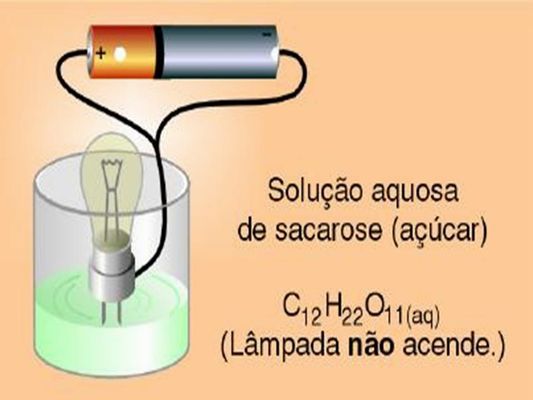
Fonte. http://www.profpc.com.br/Teoria_arrhenius.htm acessado 18/11/09
A condutividade do ácido clorídrico (HCl)
O ácido clorídrico na verdade é uma substância molecular, ou seja, os átomos de hidrogênio e do cloro se unem através de ligação covalente. Se não há íons na substância pura, como poderiamos justificar a condutividade elétrica da solução aquosa de HCl.
A explicação apresentada foi muito criativa e muito importante no futuro do desenvolvimento das pesquisas químicas. Os cátions e ânions, não existem no HCl puro, passariam a existir no mo mento em que as moléculas de HCl entrassem em cont ato com a água. A essa quebra da ligação covalente em íons chamamos de ionização.
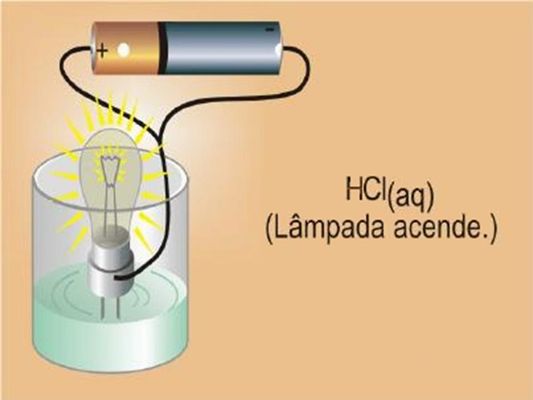
Fonte: http://www.profpc.com.br/Teoria_arrhenius.htm acessado 18/11/09
Testando a condutividade elétrica de uma solução de água destilada verificou-se que a lâmpada se manteve apagada, indicando que a água pura não conduziu corrente elétrica.
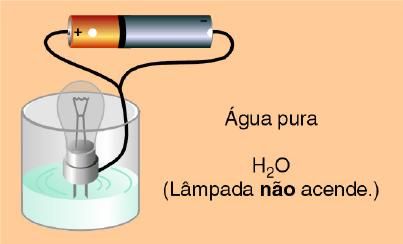
Fonte: http://www.profpc.com.br/Teoria_arrhenius.htm acessado 18/11/09
Agora que sabemos que a água destilada (pura) não conduz eletricidade, como explicar então, o fato da água potável conduzir eletricidade?
A água destinada ao abastecimento das cidades, ou seja, a água potável, é proveniente dos rios, lagos ou represas e contém dois tipos de impurezas: materiais sólidos em suspensão, como areia, restos de animais e vegetais mortos, etc., que geralmente se separam quando a água permanece em repouso e materiais que não se separam nestas condições, como bactérias, substâncias solubilizadas, sais solúveis, etc.
Esta água sofre um processo de tratamento físico e químico, que envolve etapas tais como: floculação, decantação, filtração e desinfecção, onde são adicionadas várias substâncias químicas com a finalidade de deixar a água em condições de ser consumida pela população. Estas substâncias químicas dissolvidas na água originam íons, que são responsáveis pela condutibilidade elétrica desta solução.
1) Explicar os conceitos de indicadores ácidos bases a partir de situações casuais
 Indicador de ácido e base na cozinha da minha casa
Indicador de ácido e base na cozinha da minha casa
Fonte: http://portaldoprofessor.mec.gov.br/storage/recursos/17327/Web/labvirtq/simulacoes/tempUpLoad/sim_qui_indicadores.htm acessado 18/11/09
Após assistir ao simular sugerimos:
- Uma discussão sobre o conceitos apresentados.
- Análise dos produtos químicos estudados na aula, comparando com os do simulador.
- Diálogo com os alunos sobre as situações do cotidiano que envolvem química.
- Produção de texto, onde os estudantes expressem o seu entendimento do tema da aula e sua aplicabilidade no cotidiano, abordando também sobre os preconceitos que possuímos, ou seja, quais os conhecimentos do senso comum que são estudados nas aulas de química.
REFERÊNCIAS:
LEMBO; Química Reali dade e Contexto. São Pa ulo: Editora Ática, 1º Edicação / 6º Impressão 2004
Atkins, P.; Jones, L. Princípios de química: question ando a vida moderna e o meio ambiente. Editora Bookman, 2001.
SARDELLA, Antonio; Curso Completo de Química. São Paulo: Editora Ática, 2º Edição 1999
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Indicador de ácido e base na cozinha da minha casa | Animação/simulação |
Recursos Complementares

Video sobre acidos e bases, Concorreu ao concurso de VideoClip de química no ano de 2007. O grupo ficou em 3 lugar no concurso do Colégio Máxi.
Fonte. Youtube . http://www.youtube.com/watch?v=kWuR_XV8S2M acessado 18/11/09
Avaliação
A avaliação será realizada no decorrer das atividades, inicialmente observando a formação de conceitos dos estudantes, analisando seus questionamentos e intervenções, procurando, através do diálogo, perceber se houve apropriação dos conteúdos propostos e uma mudança de postura frente às questões levantadas, no que se refere à superação de idéias preconcebidas. O professor acompanhará fazendo leitura das produções dos estudantes, sugerindo as intervenções necessárias, incentivando leituras e a retomada de conteúdos, se necessário. Sugerimos que os textos produzidos pelos estudantes sejam divulgados no edital da sala.
Cinco estrelas 1 classificações
- Cinco estrelas 1/1 - 100%
- Quatro estrelas 0/1 - 0%
- Três estrelas 0/1 - 0%
- Duas estrelas 0/1 - 0%
- Uma estrela 0/1 - 0%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
Cheila Costa Silva, E. E. Prefeito José Franco de Gouveia , Minas Gerais - disse:
cheilacosta@yahoo.com.br14/12/2011
Cinco estrelasexcelente recurso vsual e muito bem explicada.
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


