27/01/2010
Edson Luis Nunes, Daniel Rodrigues Ventura, Isnard Domingos Ferraz, José Ângelo de Faria.
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Física | Calor, ambiente e usos de energia |
O que o aluno poderá aprender com esta aula
Entender a transformação isotérmica e a importância dela no estudo das máquinas térmicas convencionais, bem como no entendimento da Máquina de Carnot.
Entender a transformação isotérmica e a importância dela no estudo das máquinas térmicas convencionais, bem como no entendimento da Máquina de Carnot.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Temperatura na escala Absoluta (ou Kelvin), calor, pressão, volume, Lei de Boyle, gases perfeitos e 1a Lei da Termodinâmica.
Estratégias e recursos da aula
Comece dizendo aos alunos que o estudo das transformações termodinâmicas é necessário para o entendimento do funcionamento de máquinas térmicas como geladeiras, motores de combustão interna, usinas nucleares e termo-elétricas, entre outras. Diga depois que, das transformações termodinâmicas particulares que serão estudas, a isotérmica é uma das duas mais importantes para se entender o funcionamento das máquinas térmicas ditas convencionais, além de permitir também o entendimento da Máquina de Carnot, que é uma máquina térmica especial estudada posteriormente, e servirá de referência para medições de rendimento das máquinas térmicas em geral.
Faça então uma breve revisão sobre a Lei de Boyle. Depois faça a seguinte sequência de perguntas para os alunos. Entre colchetes está uma das prováveis respostas corretas apenas para orientação do professor. Após cada uma das perguntas deixe que interajam entre si com o objetivo de chegarem à provável resposta correta usando apenas o conhecimento do dia-dia que já possuem do assunto, bem como o conhecimento teórico já fornecido pelo professor sobre o conteúdo. Depois, se necessário, discuta mais a resposta correta com eles para acrescentar outras informações importantes que por ventura ainda não tenham sido esclarecidas.
1) suponha um recipiente de volume facilmente variável (dotado de êmbolo móvel). O que acontece com um gás, contido nesse recipiente, quando se fornece uma certa quantidade Q de energia térmica para o gás? [o gás aumenta de volume...]
2) suponha agora que, sobre este êmbolo há um objeto, um tijolo, por exemplo. Com o deslocamento do êmbolo este tijolo será movido para cima, ou seja, ele receberá trabalho. Suponha também que não houve variação da temperatura do gás. Pergunta-se, o que aconteceu com a energia Q fornecida ao sistema? [transformou-se em trabalho realizado sobre o tijolo...]
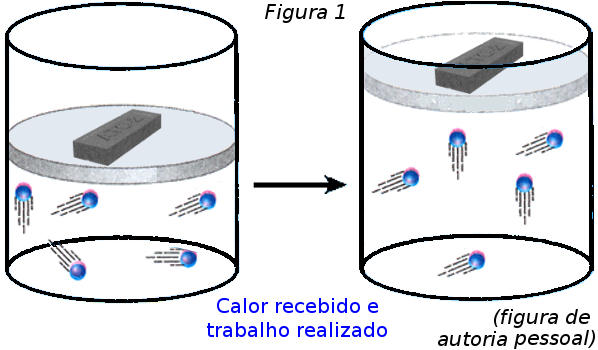
Explique agora para eles o que acontece com o sistema, esquematicamente, por intermédio da Figura 1. Depois, matematicamente, à luz da 1a Lei da Termodinâmica, usando os passos abaixo:
a) se não houve variação de temperatura então ΔU = 0 (não houve aumento na temperatura do gás);
b) a energia Q que entrou no sistema, como não provocou a variação de energia interna, foi toda entregue ao meio externo realizando-se trabalho sobre o meio (elevação do tijolo);
c) matematicamente, o que aconteceu pode ser calculado da seguinte maneira:
ΔU = Q – τgás → 0 = Q – τgás → Q = τgás.
Dê agora em exemplo de aplicação prática.
Diga aos alunos que esta transformação é uma isotérmica e é o que acontece, aproximadamente, quando se infla um balão de festas. O ar proveniente de seus pulmões possui temperatura constante. À medida que você vai enchendo o balão ele vai aumentando de volume estando o ar em seu interior à uma mesma temperatura.
Diga também que esta transformação acontece nas máquinas térmicas convencionais e na Máquina de Carnot, por duas vezes durante a realização de um ciclo.
Peça a eles agora para discutirem entre si o processo inverso, ou seja, levando-se em consideração o mesmo recipiente, o que acontece quando se fornece trabalho para o sistema provocando-se a redução de volume do recipiente sem aumento da temperatura do gás. Peça para usarem a seguinte con venção:
-- trabalho realizado p elo sistema é positivo (τgás > 0);
-- trabalho recebido pelo sistema é negativo (τgás < 0);
-- calor recebido pelo sistema é positivo (Q > 0);
-- calor f ornecido pelo sistema é negativo (Q < 0).
Analise depois os resultados a que eles chegaram ao final das discussõe s. É preciso que concluam que, no processo inverso Q = τgás e ΔU = 0 , mas Q < 0 e τgás < 0. Se não chegarem a essa conclusão o professor deve intervir e conduzi-los a ela mostrando a Figura 2.
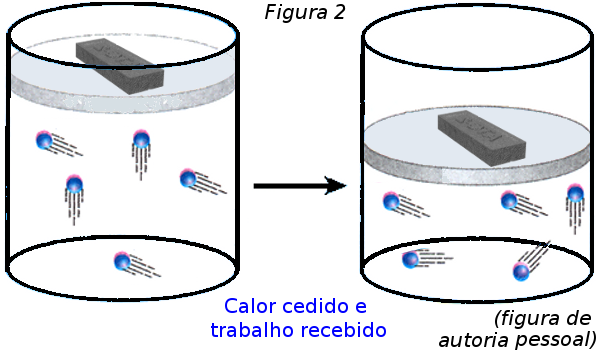
Para finalizar discuta comparativamente, à luz da convenção citada, que no primeiro caso Q e τgás têm sinais positivos (Q > 0, pois o sistema recebeu calor e, τgás > 0, pois o sistema realizou trabalho) e que na situação inversa Q e τgás têm sinais negativos (Q < 0, pois o sistema cedeu calor e, τgás < 0, pois o sistema recebeu trabalho).
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Transformações gasosas | Animação/simulação |
Recursos Complementares
Aprenda mais sobre a Transformações isotérmicas:
BrasilEscola: http://www.brasilescola.com/fisica/principio-termodinamica.htm
Simulador Stefanelli : http://www.stefanelli.eng.br/webpage/simtermo/p_sim_tp.html
Wikipedia : http://pt.wikipedia.org/wiki/Termodin%C3%A2mica
NEWTON, V.B; HELOU, R.D.; GUALTER, J.B. Tópicos de Física 2 – Termologia, Ondulatória e Óptica. São Paulo: Editora Saraiva, Vol. 2, 448p., 18a Ed., 2007.
Avaliação
Elabore questões teóricas e práticas sobre esse assunto. Nas questões teóricas explore a relação entre pressão e volume quando não há variação na temperatura do gás contido no recipiente dotado de êmbolo móvel. Nas questões práticas faça os alunos realizarem cálculos que envolvam a equação que explica matematicamente a 1a Lei da Termodinâmica quando aplicada a transformações isotérmicas, tanto de compressão quanto de expansão.
Quatro estrelas 1 classificações
- Cinco estrelas 0/1 - 0%
- Quatro estrelas 1/1 - 100%
- Três estrelas 0/1 - 0%
- Duas estrelas 0/1 - 0%
- Uma estrela 0/1 - 0%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
Jurandir Rodrigues de Moraes, EEFM GOV. MANOEL DE CASTRO FILHO , Ceará - disse:
jurandirmoraes2008@gmail.com24/03/2010
Quatro estrelasA aula de de José Marcelo Gomes sobre termodinâmica foi bastante atrativa devido iniciar com conhecimentos prévios sobre as aplicações no cotidiano como: as geladeiras, os motores a combustão interna, entre outros e explicou a relação do calor com a realização de trabalho em transformações isométrica juntamente com as leis da termodinâmica.
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus



