19/03/2009
| Modalidad / Nivel de Enseñanza | Disciplina | Tema |
|---|---|---|
| Ensino Médio | Química | Transformações: caracterização, aspectos energéticos, aspectos dinâmicos |
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
O que o aluno poderá aprender com esta aula
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Estratégias e recursos da aula
Ésteres são substâncias presentes em nosso cotidiano. Desde um simples perfume de uma flor ou fruta até as gorduras. O experimento a seguir é simples, de baixo custo, obtendo um éster com odor semelhante ao do conhecido Gelol.
A seguir, o roteiro do experimento como ele é apresentado ao aluno.
Atividade de Laboratório
* Título: Reação de Esterificação
* Objetivo: Mostrar obtenção de um éster a partir de uma substância bem conhecida: a aspirina.
* Materiais e Reagentes: agarrador, conta-gotas, erlenmeyer, lamparina ou bico de bunsen, tubos de ensaio, gral e pistilo; álcool comum, ácido sulfúrico concentrado, ácido acetil salicílico (comprimido de aspirina, A.A.S., etc.).
* Procedimento: Síntese do Salicilato de Etila
Procedimento: Em um tubo de ensaio grande coloque 20 ml de etanol e adicione (cuidado!) 40 gotas de ácido sulfúrico concentrado.
Pulverize um comprimido de ácido acetil salicílico em um almofariz (gral). Coloque-o no tubo de ensaio. Anote o odor.
Aqueça por cerca de 15 segundos tomando cuidado para que a mistura reacional não ebula.
Deixe o tubo de ensaio na estante por cinco minutos para resfriar um pouco. Você percebe algum odor?
Coloque água em um erlenmeyer.
Despeje o conteúdo do tubo de ensaio nesse erlenmeyer. Percebe algum odor?
A reação que você acabou de fazer é chamada de esterificação.
Ela pode ser equacionada assim:
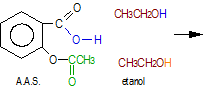
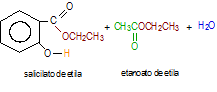
Questões:
1. Qual o odor do salicilato de etila?
2. Identifique os grupos funcionais dos reagentes nessa reação.
3. Qual a finalidade do ácido sulfúrico nessa reação?
4. Por que pulverizamos o comprimido?
________________
Algumas considerações:
1) O rendimento da reação é melhor se antes e depois do aquecimento, o tubo de ensaio for agitado. Basta bater algumas vezes o tubo de ensaio contra a palma da mão.
2) Enquanto o tubo de ensaio estiver aquecido, não conseguimos identificar o cheiro de Gelol. Por isso, fazemos o resfriamento jogando toda a mistura reacional em um erlenmeyer contendo água de torneira. Embora possamos usar outro frasco, o erlenmeyer é interessante pois sua forma cônica permite conduzir melhor o odor às narinas.
3) Pode-se notar uma certa oleosidade na água assim que recebe a mistura reacional, evidenciando que a formação do produto foi bem sucedida.
4) Na verdade, o gelol é constituído por salicilato de metila e não o salicilato de etila. A diferença é mínima. Para obter o salicilato de metila seria necessário substituirmos o etanol pelo metanol. Além de ser mais caro e mais difícil de conseguir do que o etanol, o metanol é uma substância bem mais tóxica.
5) O etanol usado não precisa ser puro. Usamos álcool etílico com no mínimo 92 ºGL.
6) O ácido acetil salicílico (aspirina) também é um éster. É uma ocasião para mostrar que a Química possui várias soluções ou caminhos. Nesse caso, fugimos do exemplo mais difundido que é obter éster reagindo álcool com ácido carboxílico.
Avaliação
Quatro estrelas 6 calificaciones
- Cinco estrelas 3/6 - 50%
- Quatro estrelas 3/6 - 50%
- Três estrelas 0/6 - 0%
- Duas estrelas 0/6 - 0%
- Uma estrela 0/6 - 0%
Denuncia opiniones o materiales indebidos!
Opiniones
-
Ronaldo da Luz Silva, Colégio Estadual Cristo Rei - Ensino Normal. , Paraná - dijo:
rndlquimica@hotmail.com02/07/2014
Cinco estrelasÓtima atividade experimental!
-
Alexandre Rodrigues Soares, COL ESTADUAL PROFESSOR NICOLAU CHIAVARO NETO , Rio Grande do Sul - dijo:
khemis@bol.com.br14/04/2012
Cinco estrelasObrigado pelos comentários. Uma dica para tornar mais prática e segura a experiência é disponibilizar aos alunos o ácido sulfúrico em frascos conta-gotas de vidro ou plástico (daquelas usadas em remédio). Costumo usar as de plástico. Com o passar dos dias, o ácido sulfúrico ataca borracha e plástico, por isso, evite usar esses recipentes para armazenar o ácido sulfúrico.
-
marcelo, SESI , São Paulo - dijo:
mckarvalho@gmail.com13/04/2011
Quatro estrelasGostei muito da sequencia didática. Sou professor de Química e vou aplicar esse experimento com minhas turmas de 3° ano do médio. Depois, volto aqui e digo como foi. abraços
-
Edemilson Luis de Andrade, Escola Lauro Müller , Santa Catarina - dijo:
edemilson.luis@gmail.com27/08/2010
Cinco estrelasEsta experiência me ajudou muito para elaborar meu trabalho de aula experimental.
-
Amannda E. S. A. Hadjhffy , sao camilo de lelis , Espírito Santo - dijo:
amanndinha@hotmail.com24/03/2010
Quatro estrelasÓtimo, de bom valor teórico e muito bem explicado. Meus parabéns.....
-
Maria Goretti Bernardes, Instituto de Educação Estadual de Maringá , Paraná - dijo:
mariagoretti01@brturbo.com.br24/03/2010
Quatro estrelasÓtimo
- Sugerencias de clases
- Clases
- Colecciones de clases
- Crear clase
- Crear individual
- Crear em equipo
- Accede tus equipos
- Mis clases
- Orientaciones
- Creando equipos
- Pistas para producción de clases
- Reflexiones pedagógicas
- Utilizando la herramienta
- Artículo: portal educacional
- Estadísticas de uso del Portal
- Clases Estadísticas
- Estadísticas de recursos
- Estadísticas de visitas
- Recursos utilizados en las clases de
- Reflexiones pedagógicas
- Informaciones de cursos
- Cursos
- e-Proinfo
- Materiales de curso
- Materiales de estudio
- Artículos y Publicaciones
- Asuntos relevantes
- Opiniones
- Ciencias de la vida cotidiana
- Destaca Internacional
- Consejos prácticos
- La educación profesional y tecnológica
- Entrevistas
- Estrategias pedagógicas
- Las innovaciones tecnológicas
- Los materiales del curso
- Acontecimiento Materiales
- Directrices y directivas
- Parámetros y referencias
- Programas en los vídeos
- Tutoriales
- TVescola
- Cuadernos didáticos
- Colecciones de recursos
- Recursos educacionales
- Sitios temáticos
- Tv escuela en vivo
- Herramienta del portal
- Foro
- Portal em Youtube
- Compartiendo presentaciones
- Herramientas por internet
- Blog
- Compartir videos
- La comunicación en línea
- Crear y compartir presentaciones
- Editar y compartir fotos
- Escritura colaborativa
- Únete a una comunicade
- Hilo
- Organizar y compartir tus favoritos
- Podcast
- Radio / TV y otra universidad
- Redes Sociales
- Robot Ed
PLATAFORMA FREIRE
- Bibliotecas
- Proinfo integrado de capacidad
- cultura
- Diccionarios, traductores y enciclopedias
- La educación inclusiva
- Geoprocessamentos
- La inclusión digital
- Infografía
- Juegos educativos
- Periódicos
- Museos
- Observatorios y planetarios
- Organizaciones gubernamentales
- Las plataformas educativas
- Portales educativos y otros
- MEC Portal
- Profesores Premio de Brasil
- Producciones de los docentes
- Proyectos de Escuelas
- Proyectos innovadores
- Los proyectos sociales y educativos
- Escuela de Radio
- Recursos digitales
- Revistas
- Búsqueda Sitios
- Sitios portal temático y TVescola
- Software de edición y otros
- Software educativo
- Un ordenador por alumno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


