23/05/2010
Marco G. B. Burlamaqui
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
O que o aluno poderá aprender com esta aula
- Conceituar forças intermoleculares;
- Conceituar e diferenciar as interações intermoleculares;
- Descrever como ocorrem as ligações de hidrogênio;
- Identificar os modelos das forças intermoleculares.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
- Ligação iônica;
- Representação das ligações iônicas;
- Identificação da quantidade de elétrons na camada de valência através da distribuição eletrônica;
- Eletronegatividade;
- Polaridade das moléculas.
Estratégias e recursos da aula
Professor, essa aula foi planejada para ser executada em um laboratório de informática, onde os alunos deverão ser divididos em grupos de no máximo três alunos, mas caso a escola não possua tal recurso, o professor poderá utilizar um computador e um data show para apresentar as simulações e imagens para os alunos. Ao longo da descrição da aula serão apresentadas alternativas para o desenvolvimento da mesma.
Leve para a sala de aula ou salve nos computadores as figuras 1 e 2 apresentadas na parte de introdução da aula. Providencie também material para a confecção de cartazes.
Aula 1:
Professor, inicie a aula levando os alunos para o laboratório de informática da escola. Divida a turma em grupos de três alunos, em seguida, revise os conceitos sobre interações das cargas: cargas opostas se atraem e cargas iguais se repelem (isso também poderá ser feito em parceria com o professor de Física da sua escola).
Após isso, informe aos alunos que as ligações químicas são modelos das interações que existem nos átomos para formar as moléculas, como por exemplo, a molécula de ácido clorídrico que possui fórmula molecular HCl e que o modelo da ligação iônica explica as interações entre os átomos de cloro e hidrogênio.
Em seguida, faça as seguintes perguntas aos alunos:
1 – Quantas moléculas existem em um grão de sal?
2 – Como essas moléculas se unem?
Para responder as questões propostas os alunos deverão pesquisar preferencialmente nos sites abaixo:
http://www.qmc.ufsc.br/qmcweb/artigos/forcas_intermoleculares.html
http://www.infoescola.com/quimica/forcas-intermoleculares-van-der-waals-e-ponte-de-hidrogenio/
Em função dos conhecimentos prévios dos alunos é provável que eles respondam que em um grão de sal existem inúmeras moléculas. Agora, em relação à segunda questão, as respostas serão baseadas nos modelos das ligações químicas, como por exemplo, o modelo das ligações iônicas.
Em seguida mostre as imagens da lagartixa e do mosquito na água. Informe aos alunos que no final da aula eles poderão explicar como a lagartixa anda na parede e como o mosquito flutua na água.
Figura 1 – Lagartixa sobre um objeto
Fonte: http://www.labec.com.br/biodigital/wordpress/wp-content/uploads/2008/12/lagartixa_mexilhao.jpg. Acessada em 10 de abril de 2010
Figura 2 – Mosquito sobre a água
Fonte: http://www.wldelft.nl/gen/waterfacts/im/water-mosquito.jpg. Acessada em 10 de abril de 2010
Informe aos alunos, que os químicos desenvolveram formas de determinar as interações entre as moléculas. Em seguida, os alunos deverão pesquisar na internet e responder a segunda questão proposta anteriormente. Caso esteja trabalhando sem o laboratório de informática, essa pesquisa poderá ser feita utilizando os livros didáticos e a biblioteca da escola. Com a pesquisa os alunos deverão responder as questões abaixo:
1 – Quais são os modelos que explicam as interações entre as moléculas?
2 – Explique como ocorre cada um desses modelos.
Os alunos responderão com facilidade essas questões. Informe aos alunos que cada grupo deverá entregar para o professor a atividade anterior para compor a avaliação.
Após a pesquisa, escolha dois ou três grupos para que leiam as suas respostas para os demais alunos. Em seguida, explique aos alunos que as interações entre as moléculas são chamadas de interações de Van der Waals, em homenagem ao cientista holandês Johannes D. Van der Waals, autor da formulação matemática que permitiu o desenvolvimento desse estudo.
Depois disso, peça para que os alunos abram a simulação abaixo:
Ligações dipolo instantâneo-dipolo induzido
http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=10686
 Ligações dipolo instantâneo-dipolo induzido
Ligações dipolo instantâneo-dipolo induzido
Figura 3 – Representação das ligações covalentes na molécula de oxigênio
Fonte: Tela da simulação
Os alunos deverão explicar como ocorre a interação dipolo-dipolo, para isso deverão utilizar os conceitos apresentados na simulação e as informações pesquisadas anteriormente. Em seguida, explique para os alunos que quando ocorre a aproximação de duas ou mais moléculas, os elétrons de suas camadas de valência, incluindo os participantes de ligações covalentes, são influenciados pelos átomos das moléculas vizinhas. Com isso, uma nova distribuição das cargas elétricas, gerando um dipolo induzido. Esse tipo de interação ocorre com as moléculas apolares, e por isso recebe o nome de dipolo induzido, pois as moléculas apolares não possuem dipolo.
Professor, caso a escola não possua o laboratório de informática, poderá projetar a simulação com um auxílio de um data show e um computador, ou ainda utilizar imagens para explicar como ocorre o dipolo induzido.
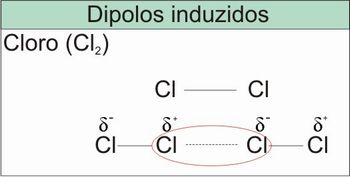
Figura 4 – Representação dos dipolos induzidos em moléculas de cloro
Fonte: elaborada pelo autor
Após a atividade, pergunte aos alunos como ocorrem as interações entre as moléculas polares? É provável que as respostas dos alunos sejam baseadas na pesquisa feita anteriormente.
Depois de ouvir as respostas dos alunos, informe que a interação dipolo-dipolo ocorre nas moléculas polares, pois essas moléculas possuem dipolos elétricos permanentes.
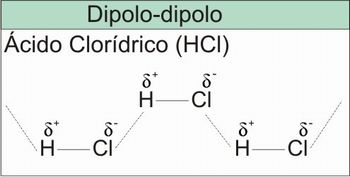
Figura 5 – Representação da interação dipolo-dipolo das moléculas de HCl
Fonte: elaborada pelo autor
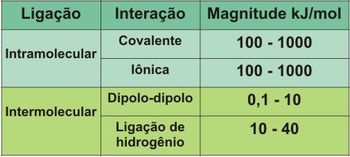
Em seguida, explique aos alunos que um tipo especial da interação dipolo-dipolo ocorre em substâncias que possuem átomos de hidrogênio ligados a átomos de flúor, oxigênio ou nitrogênio. Mostre a tabela abaixo para os alunos e pergunte a diferença entre as interações dipolo-dipolo e a ligação de hidrogênio.
Tabela 1 – Magnitude das interações intramolecular e intermolecular
Fonte: http://www.qmc.ufsc.br/qmcweb/artigos/forcas_intermoleculares.html. Acessado em 10 de abril de 2010.
Aula 02:
Nesta aula divida a turma em 5 grupos. Os alunos não precisam ser deslocados dos seus lugares, basta o professor indicar o seu novo grupo. Cada grupo deverá fazer uma pesquisa sobre o assunto e confeccionar cartazes para apresentar para a turma:
Grupo 1 – Interações dipolo-dipolo induzido
Grupo 2 – Interações Dipolo-dipolo
Grupo 3 – Ligações de hidrogênio
Grupo 4 – Explicar o caso da lagartixa
Grupo 5 – Explicar o caso do mosquito na água
Reserve um tempo para que cada grupo pesquise o assunto, e depois deixe que eles se reúnam para criar uma forma de apresentar para os demais alunos, sugira a confecção de cartazes para facilitar a explicação. Eles deverão descrever os modelos apresentados na aula.
Aula 3:
Nessa aula será feito um experimento demonstrativo sobre a tensão superficial da água. Para isso, se posicione em um local visível e peça para que os alunos observem e facão anotações sobre o experimento.
Roteiro Experimental: Rompendo a tensão superficial da água
Materiais:
• 1 prato fundo com água;
• um pouco de talco OU corante de alimento OU pedacinhos de papel;
• detergente de cozinha;
• palitos de dente.
Procedimentos:
- Coloque um pouco de água em um prato fundo e espere até que fique bem parada no prato.
- Jogue um pouco de talco na superfície da água e observe. Você pode ver que o talco não afunda na água.
- Molhe a ponta de um palito de dente com detergente de cozinha.
- Com cuidado, encoste a ponta do palito com detergente no centro do prato onde está o talco e observe com bastante cuidado. O que aconteceu com o talco?
- Faça a mesma experiência usando corante de alimento. O corante deve ser colocado com bastante cuidado na superfície da água. Agora, você vai colocar o detergente na lateral do prato e não no meio! Coloque uma gota de detergente na lateral do prato e deixe escorrer até a água.
Obs.: Você pode fazer a mesma experiência usando, ao invés do talco, pedacinhos de papel picado que devem ser jogados na superfície da água.Use dois corantes de alimento de cores diferentes. Coloque as gotas separadas e depois o detergente. Observe o que acontece.
Experimento adaptado do site http://www.bioqmed.ufrj.br/ciencia/TensaoSup.htm. Acessado em 02 de maio de 2010.
Após o experimento, os alunos deverão fazer um relatório sobre o mesmo, abordando os conteúdos trabalhados e as observações feitas. Após isso utilize as observações dos alunos para explicar a aplicação do conceito de ligações de hidrogênio no fenômeno da tensão superficial da água.
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Ligações dipolo instantâneo-dipolo induzido | Animação/simulação |
Recursos Complementares
Artigo da Revista Química Nova na Escola: Interações intermoleculares:
http://qnesc.sbq.org.br/online/cadernos/04/interac.pdf
Vídeo sobre forças intermoleculares:
http://www.youtube.com/watch?v=wYJpBBkQd4k
Site da UFSC sobre interações intermoleculares
http://www.qmc.ufsc.br/qmcweb/artigos/forcas_intermoleculares.html
Avaliação
A avaliação poderá ser em função:
- da participação dos alunos ao longa das aulas;
- pesquisas entregues pelos alunos para o professor;
- apresentação dos conteúdos propostos na segunda aula.
Sem estrelas 0 classificações
- Cinco estrelas 0/0 - 0%
- Quatro estrelas 0/0 - 0%
- Três estrelas 0/0 - 0%
- Duas estrelas 0/0 - 0%
- Uma estrela 0/0 - 0%
Denuncie opiniões ou materiais indevidos!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus