19/05/2010
Marco G. B. Burlamaqui
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
O que o aluno poderá aprender com esta aula
Conceituar os sais;
- Utilizar as regras de nomenclatura dos sais para nomear alguns sais;
- Identificar as principais classificações dos sais;
- Relacionar as características dos sais com as suas propriedades;
- Identificar as principais aplicações dos sais.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
- Ligação iônica;
- Representação das ligações iônicas;
- Propriedades químicas das substâncias e dos materiais.
Estratégias e recursos da aula
Professor, leve para a sala de aula pequenas amostras de sal de cozinha de bicarbonato de sódio e carbonato de sódio, caso queiro poderá substituir o último pelo sal que achar mais conveniente. Providencie os materiais necessários para a execução do experimento descrito na Aula 3.
Aula 1:
Professor, inicie a aula fazendo as seguintes perguntas aos alunos:
1 – O que é sal para você?
2 – Existe apenas um tipo de sal?
É provável que os alunos respondam que sal é o sal de cozinha e que eles não conhecem outro tipo de sal. Após ouvir as respostas dos alunos coloque sobre a sua mesa o sal de cozinha (cloreto de sódio), carbonato de cálcio e bicarbonato de sódio sem identificá-los. Explique que todos eles são sais, pois o sal para a maioria da população é aquele sólido branco usado no tempero de alimentos, mas para os químicos o cloreto de sódio é mais um exemplo de sais. Sal pode ser definido como um tipo de substância iônica que possui um ou mais ânions diferentes da hidroxila (OH-) e do Oxigênio (O2-) e pelo menos um cátion diferente do hidrogênio (H+).
Figura 1 – Exemplos de sais
Fonte: http://www.eca.usp.br/nucleos/njr/voxscientiae/img/carbonato_de_sodio.jpg
http://www.bsgespeciarias.com.br/imagens/bicarbonatodesodio.jpg
http://correiogourmand.com.br/images/salrefinado100.gif Acessados em 14 de abril de 2010.
Após a explicação, peça para que os alunos identifiquem bicarbonato de sódio dentre os sais apresentados. Os alunos indicarão de maneira aleatória, muitos tentarão utilizar o paladar para tentar identificar, mas alerte que muitos sais são extremamente tóxicos. Explique aos alunos que embora todas as substâncias apresentadas sejam sais, elas apresentam propriedades diferentes. Para exemplificar isso, coloque cada um dos sais em copo com água e peça para que os alunos observem. Explique que ambas as substâncias solubilizam na água, mas somente o bicarbonato de sódio tem a propriedade química de efervescência. A efervescência e a solubilidade são propriedades importantes dos sais.
Figura 2 – Efervescência do bicarbonato de sódio
Fonte: http://educa.fc.up.pt/ficheiros/categorias/68/ascor.jpg. Acessado em 14 de abril de 2010
Em seguida, leve os alunos para o laboratório de informática, ou se não for possível utilizar esse recurso, projete a simulação na própria sala de aula, com o auxílio de um data show e de um computador. Se preferir também poderá utilizar a biblioteca da escola como fonte de pesquisa.
No laboratório de informática divida a turma em grupos de três ou quatro alunos. Feito isso, peça para que os alunos abram a simulação abaixo:
O sal
http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=16872
Figura 3 – Tela inicial do recurso
Os alunos deverão utilizar a simulação para responder as perguntas a seguir:
1 – Qual a definição de sal de acordo com a simulação?
Para responder a próxima pergunta os alunos poderão utilizar as informações presentes na própria simulação, ou pesquisar, em grupo, no site abaixo:
http://www.fisica.net/quimica/resumo12.htm
2 – Pesquise e descubra o que é reação de neutralização?
3 – Quais as classificações dos sais que foram apresentadas pela simulação?
Os alunos deverão responder as questões em uma folha separada para entregar para o professor, ou então colocar as respostas em um editor de textos e salvar no computador.Após essa atividade, escolha um grupo para responder as questões para os demais alunos. Explique que as reações de neutralizações são reações que ocorrem entre ácidos e bases, originando um sal, como por exemplo, a reação entre o ácido clorídrico e o hidróxido de sódio, e temos como produto da reação o cloreto de sódio. Os sais também podem ser classificados de acordo com a natureza dos íons e de acordo com a solubilidade em água. Para que os alunos entendam melhor a classificação dos sais, proponha que eles pesquisem, na internet ou nos livros, essas classificações. Informe que eles entregar essas informações para o professor.
Aula 02:
Após a pesquisa, escreva no quadro o nome de alguns sais e a sua respectiva fórmula molecular, como por exemplo, cloreto de sódio, acetato de sódio, cloreto de potássio e outros. Peça para os alunos que façam uma relação entre o nome do sal e os elementos que compõem o sal. Ouça as opiniões de alguns alunos, em seguida, explique que o nome do sal é formado pela seguinte regra:
“nome do ânion” de "nome do cátion”
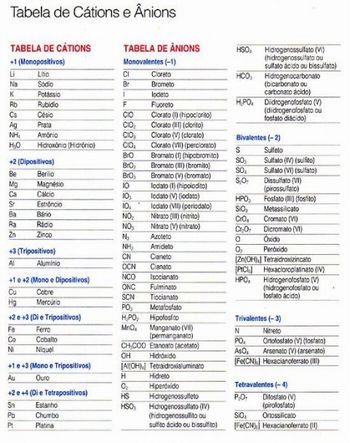
Como por exemplo, o nome do sal de cozinha que é formado pelo ânion cloreto e pelo cátion sódio, cujo nome é cloreto de sódio.Entregue ou peça para que os alunos visualizem no computador a tabela de ânions e cátions mais comuns:
Figura 4 – Tabela de Ânions e Cátions mais comuns
Fonte: http://3.bp.blogspot.com/_cNkcbKun-bA/RmS8dHaYMLI/AAAAAAAAABg/ggccCJ-SWzY/s1600-h/renato....bmp. Acessado em 14 de abril de 2010.
Eles deverão recorrer a essa tabela toda vez que tiverem dúvidas sobre a nomenclatura dos sais.
Os alunos deverão responder as questões propostas a seguir:
1 – Forneça o nome dos sais de acordo com a sua respectiva fórmula molecular:
a) KNO3 b) CaCl2 c) NaCl d) CaCO3
2 – Qual a fórmula molecular dos sais cujos nomes são:
a) Cloreto de bário b) Acetato de sódio
Professor, se desejar poderá acrescentar outros sais, de acordo com o que está trabalhando em sala de aula. Além dessa atividade, os alunos deverão pesquisar sobre as aplicações dos sais na sociedade. Esta pesquisa poderá ser entregue na mesma aula ou posteriormente, de acordo com o desenvolvimento da aula.
Aula 3:
Nessa aula os alunos farão um experimento onde serão aplicados os conceitos sobre sais. Para isso, leve os alunos para o laboratório de Química da escola. Mantenha os alunos nos mesmos grupos da aula anterior. Informe aos alunos que eles deverão fazer anotações sobre as informações feitas. Distribua os grupos nas bancadas. Fale para os alunos sobre as estalactites, se possível mostre algumas figuras.
As estalactites e as estalagmites são formações constituídas de CaCO3(s) que levam milhares de anos para se formarem no interior das cavernas. Podemos produzir estruturas semelhantes usando o NaHCO3 (bicarbonato de sódio) ou o MgSO4 (sulfato de magnésio). Essas substâncias são encontradas em farmácias.
Roteiro Experimental
Materiais
• Bicarbonato de sódio (NaHCO3) ou Sulfato de magnésio (MgSO4) — sal amargo;
• 2 frascos vazios de alimentos infantis ou copos descartáveis transparentes;
• 2 arruelas;
• 30 cm de fio grosso de lã ou barbante de algodão;
• Pires
Procedimentos
Coloque o sal escolhido nos dois frascos, preenchendo-os até a metade da sua altura. Adicione água até encher os frascos e agite os sistemas com uma colher. A seguir, amarre uma arruela à extremidade de cada fio e monte o sistema indicado na figura abaixo. Observe que você terá de colocar um pires entre os dois frascos, bem abaixo do centro do fio. Deixe o sistema em repouso por alguns dias em lugar arejado e no qual não ocorram trepidações.
Depois, responda às seguintes questões:
a) A formação das estalactites e das estalagmites em cavernas é resultado de uma reação química.
b) Nesse experimento também ocorre uma reação química?
c) Explique como se formaram as “estalactites” do experimento.
Figura 5 – Montagem do experimento
Fonte: USBERCO, João; SALVADOR, Edgard. Química – Vol. Único. Ed. 5ª. p. 176. São Paulo. Editora Saraiva. 2002
Fonte do experimento: USBERCO, João; SALVADOR, Edgard. Química – Vol. Único. Ed. 5ª. p. 176. São Paulo. Editora Saraiva. 2002
Após a execução do experimento, peça para que os alunos façam um relatório. Nesse relatório eles deverão informar os materiais que foram utilizados, os procedimentos para a execução do experimento e as observações e conclusões do grupo sobre o experimento. Cada grupo deverá entregar apenas um relatório.
Recursos Educacionais
| Nome | Tipo |
|---|---|
| O sal | Animação/simulação |
Recursos Complementares
• Artigos da Revista Química Nova na Escola: Experimentos sobre sais
http://qnesc.sbq.org.br/online/qnesc24/eeq1.pdf
http://qnesc.sbq.org.br/online/qnesc24/eeq4.pdf
• Experimento sobre separação de sais
http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=15605
Avaliação
Avalie a participação dos alunos ao longo das duas aulas. Peça para que os alunos façam um relatório das atividades desenvolvidas na sala de aula e no laboratório de informática. As atividades estão descritas na parte de sistematização da aula.
Duas estrelas 2 classificações
- Cinco estrelas 0/2 - 0%
- Quatro estrelas 1/2 - 50%
- Três estrelas 0/2 - 0%
- Duas estrelas 0/2 - 0%
- Uma estrela 1/2 - 50%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
Maisa Ramalho, Fundação Educacional Colégio Delta , Minas Gerais - disse:
avla.r@hotmail.com07/11/2010
Uma estrelanao achei ruim, deveria ter colocado a fórmula e a reação do carbonato de cálcio mais o cloreto de sódio. Ficaria mais completo. Grata.
-
roberta luciana, ifce , Ceará - disse:
betiinha.p@hotmail.com04/11/2010
Quatro estrelasadorei, ! darei está aula amanhã :D', parabéns *:
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus









 O sal
O sal