19/06/2009
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
O que o aluno poderá aprender com esta aula
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Estratégias e recursos da aula
Nessa aula busca-se explicar as cores de uma chama (ensaio de chama) interpretados segundo o modelo de Niels Bohr.
Primeiro Momento
Em sala de aula, pergunte aos alunos qual a cor do fogo. É possível que digam que seja amarela (associando com a chama de uma vela ou papel queimando). Outros, talvez digam que é azul, por lembrarem da chama no fogão. O que será que faz essas cores aparecerem na chama? E os fogos de artifício... Como funcionam? Pergunte aos alunos como essas diferentes cores podem ser explicadas à luz do Modelo de Bohr.
Segundo Momento
Leve os alunos para o laboratório de ciências, para usar o seguinte material:
a) Bico de Bunsen (ou lamparina);
b) resistor de chuveiro queimado;
c) pinça de madeira (ou um prendedor de roupas);
d) copo com água;
e) amostras de diversas substâncias (sal de cozinha ou cloreto de sódio, sulfato de cobre, bicarbonato de sódio, cal ou óxido de cálcio, permanganato de potássio).

Pegue um pedaço esticado do resistor do chuveiro. Segure-o com a pinça.
1. Molhe essa alça (haste) na água e leve-a à chama.
2. Molhe-a novamente e toque uma amostra de bicarbonato de sódio. Leve-a à chama. A chama deverá adquirir uma cor amarela.
3. Convide algum aluno para repetir os procedimentos anteriores com outra amostra. Se a alça estiver muito contaminada, substitua-a.
Convide outros alunos para fazerem o ensaio de chama. Deixe-os usarem em especial sais de cobre e de potássio que dão resultado muito bonitos e os motivam.
O vídeo abaixo mostra os resultados do ensaio de chama feito com sulfato de cobre e com permanganato de potássio, usando diferentes fontes de calor (bico de Bunsen e isqueiro). O video também exibe o ensaio usando um borrifador ("spray") no lugar da alça.
Ensaio de Chama (http://br.video.yahoo.com/watch/5086597/13502672)
Terceiro Momento
Discuta com os alunos as possíveis explicações para as diferentes cores na chama. Informe que nesses casos, as cores são características dos cátions usados. Ao serem aquecidos (receberem energia), elétrons passam para uma camada eletrônica mais externa (estado excitado). O átomo volta logo ao estado fundamental (o elétron volta para uma camada mais interna), liberando a energia recebida na forma de luz. Essas duas ideias foram propostas pelo físico dinamarquês Niels Bohr, que estudou a emissão de luz pelo hidrogênio. A cor da luz emitida pela chama depende do tipo de átomo e da temperatura atingida. Esse é o mesmo princípio de funcionamento das lâmpadas e dos fogos de artifício. Comente com os alunos que são utilizados diferentes compostos de acordo com a cor desejada nos fogos de artifício (pó de alumínio para chuva de prata; sal de bário para fogos verdes e assim por diante). Nas lâmpadas, dependendo do gás usado no bulbo, teremos cores diferentes. Peça para eles lembrarem ou observarem as lâmpadas fluorescentes, constituídas de mercúrio; lâmpadas de vapor de sódio, as de neon (ou neônio), etc.
Quarto Momento
Para compreender melhor o fenômeno do ponto de vista microscópico, leve os alunos ao laboratório de informática (ou outra forma de acesso) para trabalhar com simulações.
No RIVED, os alunos explorarão a atividade Entendendo o Átomo (http://rived.mec.gov.br/atividades/quimica/estruturaatomica/atividade4/atividade4.htm).
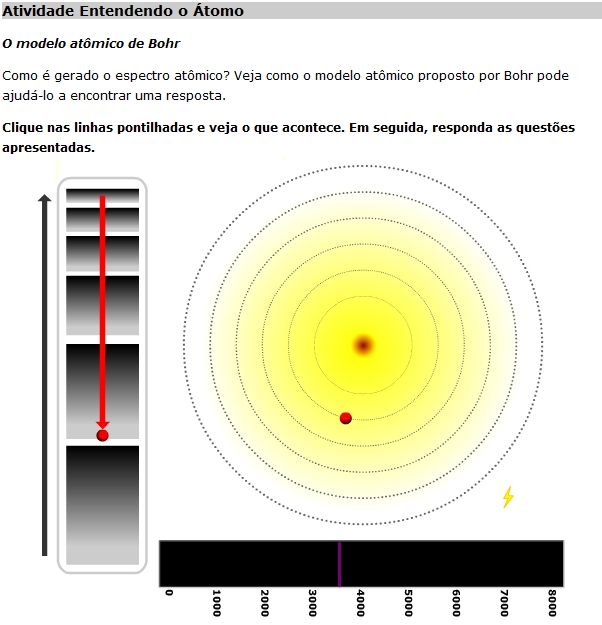
Comentários ao professor
1. A alça original para o ensaio de chama é feita de platina, um material inerte. Utilizamos o resistor de chuveiro por ser feito de liga bastante resistente. Ainda assim, a alça pode ser feita com um clipe, caso não disponha de um resistor de chuveiro. Também é possível substituir a alça e o agarrador por frascos borrifadores (frasco de desodorante tipo "spray"). Nesses casos, basta preparar as soluções com os sais. Uma em cada borrifador para evitar contaminação das soluções.
2. Caso opte por usar borrifador, experimente fazer o ensaio de chama substituindo a lamparina (ou bico de Bunsen) por um isqueiro ou mesmo uma vela. São alternativas "portáteis" que permitem constituir um kit fácil de transportar.
3. O objeto educacional do RIVED Entendendo o Átomo permite associar o modelo de Bohr a fenômenos macroscópicos como os fogos de artifício e o ensaio de chama. Esse objeto de aprendizagem apresenta imagens com resultados do ensaio de chama. Outras boas imagens podem ser pesquisadas em livros e internet. Uma alternativa à atividade O modelo atômico de Bohr (encontrada neste mesmo objeto educacional) é fazer rodar uma bola de gude em uma bacia de vidro. Segure a bacia com as duas mãos e faça movimentos circulares. Ao girar a bacia lentamente, a bola de gude ("elétron") girará próximo ao centro da bacia ("núcleo do atomo"). Girando mais rapidamente, a bola de gude gira mais afastada do centro (equivalente à absorção de energia pelo átomo).
Recursos Complementares
* Como funcionam os fogos de artifício ( http://pessoas.hsw.uol.com.br/fogos-de-artificio.htm): Texto muito bom a complementar a aula.
* A Física dos Fogos de Artifício ( http://cc.oulu.fi/~kempmp/colours.html): está em inglês, mas apresenta dados bastante interessantes.
Avaliação
Cinco estrelas 2 classificações
- Cinco estrelas 2/2 - 100%
- Quatro estrelas 0/2 - 0%
- Três estrelas 0/2 - 0%
- Duas estrelas 0/2 - 0%
- Uma estrela 0/2 - 0%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
Alexandre Rodrigues Soares, COL ESTADUAL PROFESSOR NICOLAU CHIAVARO NETO , Rio Grande do Sul - disse:
khemis@bol.com.br11/04/2012
Cinco estrelasObrigado pelos comentários, Marcia Mara Merlak Informo que o vídeo sobre ensaio de chama está agora em http://youtu.be/MvQzTnOyzMM O serviço no Yahoo foi desativado.
-
Marcia Mara Merlak, CEEBJA DOIS VIZINHOS ENS FUND MED , Paraná - disse:
marciamerlak@gmail.com13/03/2012
Cinco estrelasótimas sugestões!!!!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


