07/02/2011
Marco G. B. Burlamaqui
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
O que o aluno poderá aprender com esta aula
• Conceituar equilíbrio químico;
• Identificar como a temperatura influencia na concentração do produto e do reagente;
• Conceituar reações reversíveis e irreversíveis.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
• Reações endotérmicas e reações exotérmicas;
• Mudanças de fases;
Estratégias e recursos da aula
Professor, providencie os materiais necessários para a execução dos experimentos citados na descrição da aula. Coloque atalhos para as simulações na área de trabalho dos computadores. Providencie também uma máquina fotográfica digital que também permita filmar, para cada um dos grupos.
Aula 01:
Professor, inicie a aula no laboratório de informática. Divida os alunos em grupos de três a quatro alunos. Depois que os alunos se organizarem informe que será feito um experimento demonstrativo e que eles deverão fazer anotações para responderem algumas questões que serão colocadas no quadro.
Esse experimento pode ser feito no próprio laboratório de informática, apenas tome o cuidado de ficar em um local bem visível.
Coloque sobre a sua mesa dois béqueres de 250 ml ou dois recipientes transparentes de vidro, coloque 50 ml de água no primeiro e 50 ml de álcool no segundo. Coloque fogo no álcool. Com o auxílio de uma lamparina faça com que a água do béquer evapore.
Coloque as questões a seguir no quadro:
1 – A água que evaporou pode voltar para o seu estado inicial?
2 – O álcool (etanol) que foi queimado pode voltar para o seu estado inicial?
3 – Cite alguns exemplos de reações reversíveis e irreversíveis.
Peça para que alguns alunos leiam as suas repostas para a turma. Feito isso, utilize as respostas dos alunos e os conceitos abordados no experimento para explicar os conceitos sobre reações reversíveis (evaporação da água) e reações irreversíveis (queima do etanol).
Após essa atividade, peça para que os alunos pesquisem na internet, em grupo, sobre o significado das reações reversíveis e das reações irreversíveis. Eles deverão pesquisar preferencialmente nos sites abaixo:
http://www.mundofisico.joinville.udesc.br/PreVestibular/2005-1/mod1/node44.html
http://educar.sc.usp.br/quimapoio/equil.html
http://www.iq.ufrgs.br/ead/fisicoquimica/cineticaquimica/reacoes.html
Feito isso, peça para que os alunos abram a simulação a seguir:
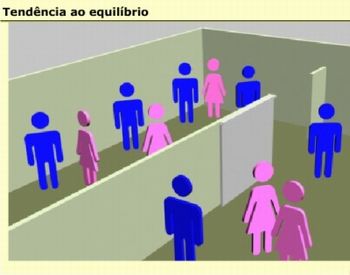
Tendência ao equilíbrio
http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=10542
Figura 1 – Tela inicial do recurso
Fonte: Retirada do recurso Tendência ao equilíbrio
Peça para que eles descrevam o que aconteceu na simulação e anote as suas observações. Para isso, eles deverão observar a quantidade de pessoas, homens e mulheres, no início e no final da simulação. Em seguida, explique que a simulação demonstra uma situação de equilíbrio, onde a quantidade de pessoas tende a ser um número constante, ou seja, um número que não muda. Em seguida, os alunos deverão abrir a simulação abaixo. Para executar essa simulação você vai precisar ter instalado em seu computador a versão mais recente do JAVA: http://java.com/pt_BR/download/windows_xpi.jsp?locale=pt_BR&host=java.com
Reações reversíveis
http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=10455
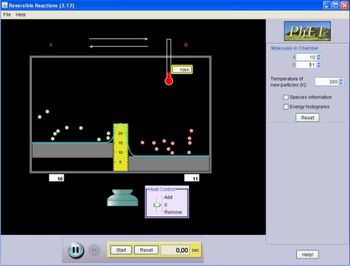
Figura 2 – Recurso Reações reversíveis
Fonte: Retirada do recurso Reações reversíveis
Explique aos alunos como eles devem manusear a simulação:
1 – Indique a quantidade de A e B, no caso coloque 10 para facilitar a visualização;
2 – Observe e anote a quantidade inicial de bolinhas de A e B;
3 – Aumente a temperatura 200 K e espere alguns segundos. Anote a quantidade de bolinhas de A e B;
4 – Diminua a temperatura em 400 K e espere alguns segundos. Anote a quantidade de bolinhas de A e B.
Informe aos alunos que o tempo que eles esperaram toda vez que ocorreu variação de temperatura foi para que o sistema entrasse em equilíbrio. Após a explicação, peça para que os alunos elaborem uma definição para equilíbrio químico, para isso, eles poderão usar as anotações da simulação anterior.
Em seguida, peça para que os alunos pesquisem na internet, em grupo, sobre a definição de equilíbrio químico. Eles deverão anotar a definição encontrada e comparar com a definição dada pelo grupo. Peça para que alguns alunos, de grupos diferentes, leiam a sua definição e a definição encontrada na internet. Para direcionar a pesquisa informe que os alunos deverão pesquisar no site a seguir: http://www.mundofisico.joinville.udesc.br/PreVestibular/2005-1/mod1/node44.html.
Professor, se necessário indique outros sites de sua preferência. Essa pesquisa será para consolidar os conceitos sobre equilíbrio químico.
Aula 2:
Leve os alunos para o laboratório de Química. No laboratório, entregue os materiais necessários para a execução do experimento, inclusive o roteiro experimental. Ao longo do experimento, um integrante do grupo deverá filmar e tirar algumas fotos.
Informe aos alunos que eles deverão fazer anotações, pois no final do experimento eles deverão fazer um relatório. Cada grupo deverá entregar apenas um relatório.
Equilíbrio Químico do íon bicarbonato
Materiais:
• Béquer de 250 mL;
• Espátula;
• Garrafa pet (600mL);
• Mangueira fina (mangueira de aquário);
• Ferro de Solda;
• Bicarbonato de Sódio;
• Indicador Vermelho de fenol;
• Água;
• Comprimidos efervescentes (Sonrisal);
• Colher.
Os procedimentos estão descritos no recurso abaixo:
Equilíbrio Químico do íon bicarbonato: Efeito da concentração
http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=25585
Caso não disponha dos materiais para a execução do experimento, você poderá exibir o vídeo abaixo, ou então salve este vídeo nos computadores e peça para que os alunos abram quando solicitado.
Equilíbrio Químico do íon bicarbonato: Efeito da concentração: parte 2: vídeo
http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=26255
Após a execução do experimento, reserve o restante da aula para que os alunos concluam o relatório. No final da aula recolha o relatório para compor a avaliação.
Aula 3
Laboratório de informática
Após a execução do experimento leve os alunos para o laboratório de informática da escola. Informe aos alunos que eles criaram um blog com as informações coletadas ao longo da aula.
Primeiramente peça para que cada grupo elabore um resumo das informações coletadas ao longo das duas aulas e organizem as fotos e os vídeos. Após a criação do blog, os alunos deverão postar as informações, as fotos e os vídeos, lembrando que os vídeos podem ser postados no YouTube e depois inseridos os links dos mesmos no blog.
Como atividade para casa, proponha aos alunos que eles comentem os vídeos e as fotos dos outros grupos. Posteriormente o professor deverá ler os comentários de cada aluno e utilizá-los para a avaliação.
Para saber como criar o blog clique nos links abaixo:
http://www.stella-science.eu/mini_units/index.php?miniunit=blog
http://www.criarumblog.com/pt/criar-um-blog-gratis/criar-blog-gratis.htm
Ajude os alunos ao longo dessa aula, de modo que cada grupo possa postar as suas idéias. Utilize este blog, para as suas aulas futuras, de modo que o conteúdo de outras aulas poderá ser colocado no blog.
Divulgue o blog por toda a escola.
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Tendência ao equilíbrio | Animação/simulação |
| Reações reversíveis | Animação/simulação |
| Equilíbrio Químico do íon bicarbonato: Efeito da concentração: parte 1: experimento prático | Experimento prático |
| Equilíbrio Químico do íon bicarbonato: Efeito da concentração: parte 2 : vídeo | Vídeo |
Recursos Complementares
• Artigo sobre o ensino de Equilíbrio Químico
http://www.quimica.ufpr.br/eduquim/eneq2008/resumos/R0420-2.pdf
Avaliação
Avalie a participação dos alunos ao longo das aulas. Avalie as atividades feitas por eles e que foram entregues para o professor.
Sem estrelas 0 classificações
- Cinco estrelas 0/0 - 0%
- Quatro estrelas 0/0 - 0%
- Três estrelas 0/0 - 0%
- Duas estrelas 0/0 - 0%
- Uma estrela 0/0 - 0%
Denuncie opiniões ou materiais indevidos!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus