19/06/2009
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
O que o aluno poderá aprender com esta aula
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Estratégias e recursos da aula
Como será que os cientistas conseguem descobrir a estrutura dos átomos sem vê-los? Nessa aula desenvolvida no laboratório de informática (ou outro ambiente com acesso a computadores), os alunos são convidados a testar diferentes modelos atômicos fazendo incidir luz sobre átomos e verificar o resultado, comparando-os com as previsões. Com esse intuito, serão usadas um software de simulação.
Primeiro Momento
Os alunos usarão o programa de simulação Modelos do Átomo de Hidrogênio (http://phet.colorado.edu/sims/hydrogen-atom/hydrogen-atom_pt.jnlp e no Portal do Professor em http://portaldoprofessor.mec.gov.br/resourceView.action?resourceIdAdmin=16657). Inicialmente, o software mostra um grande ponto de interrogação no centro de sua tela. Informe os alunos que esse ponto de interrogação seria um átomo e que iremos investigar o que acontece com a luz quando ela incide (bate) em um átomo.
Peça-lhes que "liguem" o aparelho do feixe de luz. Aparecerão círculos a representar "fótons" (http://pt.wikipedia.org/wiki/Fóton) ou constituintes da luz. Deixo-os explorarem os recursos disponíveis nesse experimento: controlando a luz ("branca" e o botão deslizante que aparece ao ativar a luz monocromática). É interessante que observem o que o espectômetro registra (há um botão para mostrá-lo).
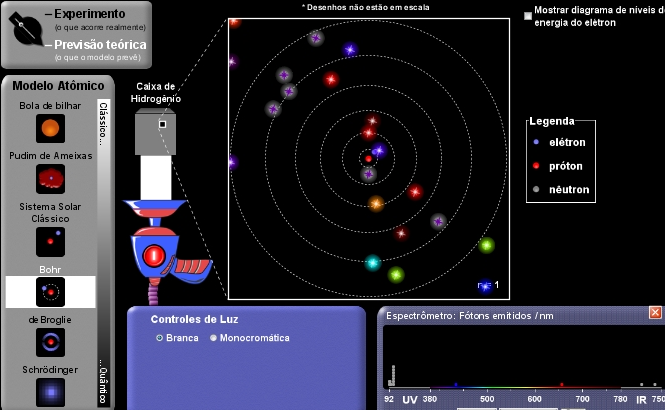
Segundo Momento
Peça aos alunos clicarem em Previsão teórica. Diga-lhes que exploraremos os quatro primeiros modelos, começando pelo "Bola de bilhar", depois "Pudim de Ameixas" (ou "Passas"), "Sistema Solar" e terminando no "Bohr".
Após explorarem cada um dos modelos, pergunte-lhes o que acontece com a luz em cada um deles. O que acontece com a luz no modelo "Bola de bilhar" é o que foi observado quando simularam o experimento? Qual a grande diferença?
O que ocorre no modelo "Pudim de Ameixas"? (para melhor entendimento, peça-lhes para colocarem uma luz monocromática amarela. Deverão notar que o fóton amarelo bate no átomo trocando de cor. Esse fenômeno previsto no modelo não é observado no experimento).
Qual o problema no modelo "Sistema Solar Clássico"? (o simulador faz os elétrons colidiram com seu núcleo. Esse colapso do átomo previsto pela Física Clássica, era a grande crítica às ideias de Rutherford).
No Modelo de Bohr, peça para o simulador mostrar o diagrama de níveis de energia do elétron. O que ocorre nas diferentes faixas de luz? Assim como devem ter feito para os outros modelos, peça-lhes para experimentarem a luz branca de diferentes cores de luz monocromática. O que ocorre quando o botão deslizante é movido entre 94 e 97? O que acontece em 103 e 122 nm?
Qual dos modelos explica melhor a simulação feita no Primeiro Momento?
Comentários ao professor
1. O programa Modelos do Átomo de Hidrogênio pode ser acessado online ou copiado ("download") para o computador. Em ambos os casos é necessário possuir Java instalado no computador. Caso a máquina não possua, será remetido a um endereço para instalá-lo. Computadores com Linux Educacional vem com java instalado e corretamente configurado.
* Online: http://phet.colorado.edu/sims/discharge-lamps/discharge-lamps_pt.jnlp
* Download: http://phet.colorado.edu/admin/get-run-offline.php?sim_id=144&locale=pt
2. Além de visualizar diferentes modelos para o átomo de hidrogênio ou explicar o que cada modelo prediz, esse simulador também pode ser aproveitado para:
* Explicar motivos para as pessoas acreditarem em cada modelo e em que cada modelo histórico era inadequado.
* Explicar a relação entre a imagem física das órbitas e o diagrama do nível energético de um elétron.
* Entender que a ciência propõe modelos e que estão em construção, sem uma verdade definitiva.
Recursos Complementares
Avaliação
Quatro estrelas 2 classificações
- Cinco estrelas 0/2 - 0%
- Quatro estrelas 2/2 - 100%
- Três estrelas 0/2 - 0%
- Duas estrelas 0/2 - 0%
- Uma estrela 0/2 - 0%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
bruna sales, g , São Paulo - disse:
bruna.sales2010@bol.com.br13/09/2010
Quatro estrelasÀ aula foii boaa
-
José Vanderlei Del Boni, E.E. Prof. Milton da Silva Rodrigues , São Paulo - disse:
jvdelboni@terra.com.br01/05/2010
Quatro estrelasExperiência de grande valor atrativo, trabalhando a parte motivacional (sensibilização) de um plano de aula, fazendo que com o educando veja o sentido no que está estudando.
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


