01/12/2010
Suelen Fernanda Machado
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Fundamental Final | Matemática | Espaço e forma |
| Ensino Fundamental Final | Ciências Naturais | Terra e universo |
| Ensino Médio | Química | Transformações: caracterização, aspectos energéticos, aspectos dinâmicos |
| Ensino Fundamental Final | Artes | Arte Visual: Produção do aluno em arte visual |
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
| Ensino Médio | Artes | Arte Visual: Contextualização |
| Ensino Médio | Matemática | Geometria |
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
O que o aluno poderá aprender com esta aula
- Compreender o que é Isomeria e a sua classificação;
- Reconhecer como ocorre a Isomeria;
- Identificar isômeros e avaliar suas implicações no comportamento de compostos de estruturas diferentes.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Os alunos devem ter conhecimento sobre: ligações químicas, classificação de cadeias carbônicas, fórmula molecular, fórmula estrutural e noções de funções orgânicas.
Estratégias e recursos da aula
Professor, para saber que conhecimentos prévios os alunos detêm sobre Isômeros, organize-os no laboratório de informática em equipes compostas por 4 pessoas.
Proponha que desenvolvam a atividade denominada Ludo Químico que está disponível em: http://www.ludoquimico.com.br/downloads/downloads.html
O Ludo Químico é um "game" de química, que tem como base o jogo indiano Pachisi. Este recurso tem como o objetivo que o aluno chegue até o final do tabuleiro respondendo corretamente as questões de química formuladas a partir dos "Parâmetros Curriculares Nacionais do Ensino Médio"e que aparecerem pelo percurso.
Ao acessar o jogo, o aluno deve efetuar a leitura das regras disponíveis no próprio recurso, jogar e anotar no caderno as respostas.
Ao final da aula deve retornar ao jogo, responder novamente as questões de modo a saber que conhecimentos apropriaram. Na realização da atividade o professor deve observar os alunos e fazer anotações no caderno de maneira a reorganizar seu planejamento se necessário.
Na sequência, indague os alunos questionando: O que caracteriza a isomeria plana? Aguarde que façam interações entre si. Pode ocorrer que saibam a resposta. Para que não haja dúvidas explique que é caracterizada quando os isômeros podem ser identificados apenas por meio de fórmulas estruturais planas.
Retome a reflexão fazendo o seguinte questionamento: Quando a isomeria é identificada como espacial? De igual modo espere que interajam entre si e que respondam. Conclua enfatizando que é somente quando podem ser identificados por meio de fórmulas espaciais.
Professor organize os alunos no laboratório de informática. Antes de propor que desenvolvam esta atividade utilize a TVPendrive ou a TV Multimídia e mostre a imagem abaixo para os alunos e discorra que Berzelius realizou sua primeira pesquisa desenvolvendo a análise de minerais em águas naturais e foi pioneiro em experimentos com eletroquímica. Para conhecer a TV Pendrive segue o link do tutorial (áudio) que está disponível em:
http://www.diaadia.pr.gov.br/tvpendrive/arquivos/File/tutoriais/tuto1.avi Acesso em: 22. set. 2010.
Fonte: http://pt.wikipedia.org/wiki/Ficheiro:J%C3%B6ns_Jacob_Berzelius_from_Familj-Journalen1873.png Acesso em: 22. set. 2010.
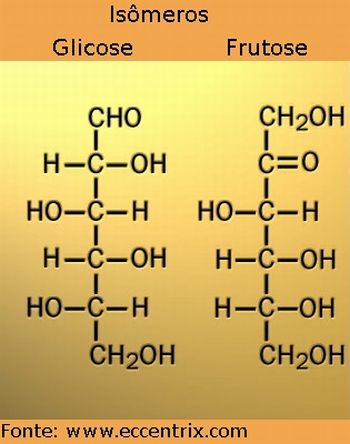
Retome o conceito de Isômeros. Explique aos alunos que estes são compostos orgânicos que possuem a mesma fórmula molecular, mas diferentes fórmulas estruturais. A palavra Isômeros deriva do grego (iso = igual; méros = parte); significa "mesma composição". Para melhor compreensão mostre a imagem dos Isômeros Glicose e Frutose e explique como está organizada a estrutura das fórmulas.
Fonte: http://www.diaadia.pr.gov.br/tvpendrive/arquivos/File/imagens/2quimica/7isoglifru.jpg Acesso em: 22. set. 2010.
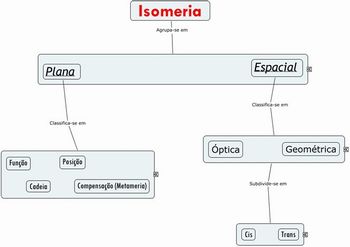
Como é classificada a Isomeria?
A Isomeria é classificada em: Plana e Espacial.
Isomeria Plana: é por meio da representação plana (fórmula estrutural plana) das moléculas das diferentes substâncias que se pode efetuar a identificação deste modelo de isomeria. Há vários tipos de isomeria plana. Sua identificação fica atrelada ao tipo de questionamento que se faz, o que exige um conhecimento elaborado sobre funções orgânicas (álcool, cetona, amina, etc.) e de classificação de cadeias carbônicas (aberta ou fechada, homogênea ou heterogênea etc.).
- Isomeria de Cadeia: os isômeros pertencem a uma mesma função química com cadeias carbônicas diferentes.
- Isomeria de Posição: são isômeros que apresentam a mesma função química, mesma cadeia carbônica e que diferem pela posição de um grupo funcional, radical ou insaturação.
- Isomeria de Função: nesta modalidade os isômeros pertencem a funções diferentes.
- Isomeria de Compensação ou Metameria: neste tipo os isômeros têm a mesma função química, com cadeias heterogêneas, que diferem pela localização do heteroátomo nas cadeias.
- Tautomeria ou Isomeria Dinâmica: neste tipo se constitui um caso particular de isomeria funcional. Os isômeros pertencem a funções químicas diferentes, cujas características de um deles é mais estável que o outro.
Isomeria Espacial: os isômeros têm a mesma fórmula molecular e fórmula espacial diferente. Existem dois casos de isomeria espacial: Geométrica ou Cis – Trans e Óptica.
- Isomeria Geométrica: neste tipo o composto apresenta isomeria geométrica ou cis-trans quando têm dupla ligação carbono-carbono, e ligantes diferentes a cada carbono da dupla ligação. Os isômeros cis e trans diferem pela fórmula espacial. No isômero cis, os ligantes iguais ficam do mesmo lado do plano da dupla ligação ocorrendo o contrário com o isômero trans.
Atividade 1 - Trabalhando com as fórmulas
Professor disponibilizamos algumas imagens a seguir é possível demonstrar aos alunos a estrutura das fórmulas dos compostos. Organize os alunos no laboratório de informática e solicite que ocupem os computadores disponíveis. Oriente para que acessem os recursos que indicamos. A partir de cada imagem, explique sobre o composto químico ao mesmo tempo, permita aos alunos que façam interações entre seus parceiros.
Etano: hidrocarboneto (saturado) alifático denominado alcano que contém mais de um átomo de carbono. É um gás que não apresenta cor e ou cheiro. Na área industrial é importante pela conversão em etileno. Em escala industrial, é produzido a partir do gás natural e do refino do petróleo.
Disponível em: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=10793 Acesso em: 22. set. 2010.
Fórmula molecular: C2H6
Metano: um gás incolor, sua molécula é tetraédrica e apolar, de pouca solubilidade na água e, quando adicionado ao ar se transforma em mistura de alto teor inflamável. É o mais simples dos hidrocarbonetos.
Disponível em: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=10706 Acesso em: 22. set. 2010.
Link: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=13893 Acesso em: 22. set. 2010.
Fórmula molecular: CH4
Propano: é um alcano que apresenta três átomos de carbonos. Algumas vezes derivado de outros produtos do petróleo, durante processamento de óleo ou gás natural. Link: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=10734 Acesso em: 22. set. 2010.
Fórmula molecular: C3H8
Butano: é um derivado do petróleo. É um gás incolor, inodoro e altamente inflamável. É um hidrocarboneto gasoso, obtido do aquecimento lento do petróleo. É o nosso gás de cozinha. Link: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=13885 Acesso em: 22. set. 2010.
Fórmula molecular: C4H10
Solicite a cada equipe que crie fórmulas estruturais a partir dos seguintes compostos: C4H10O (4 álcoois e 3 éteres); C4H8 (5 hidrocarbonetos, sendo 2 cíclicos).
Após concluírem, o professor pode efetuar a correção no quadro. Na sequência, o professor solicita as mesmas equipes que pesquisem dois compostos químicos, construam suas fórmulas utilizando os mesmos números de átomos. As estruturas obtidas devem ter estruturas em diferentes formatos. Resposta: Certamente obterão inúmeras estruturas. Igualmente o professor pode efetuar a correção no quadro para eliminar dúvidas.
Atividade 2
Esta atividade deve ser realizada por todos alunos para que o conhecimento seja uniforme. Têm como objetivo levar o aluno a aprender sobre a descoberta e o conceito químico de Isomeria, seus autores, os pressupostos científicos e filosóficos e ainda sobre suas aplicações no cotidiano.
A atividade pode ser desenvolvida em casa, na sala de aula, na biblioteca ou no laboratório de informática. Para desenvolvê-la, os alunos devem ser organizados em cinco equipes.
Equipe 1. Elaborar um texto curto e objetivo sobre a descoberta da isomeria: como se deu, quem estava envolvido, quais os pressupostos científicos e filosóficos, como era a sociedade na época.
Para que a aula seja aproveitada ao máximo e os alunos não se distraiam diante de tantas informações disponíveis na Rede indicamos alguns sites em que estão disponíveis informações sobre Isomeria.
Disponível em: http://guiadoestudante.abril.com.br/estude/simulados/quimica-isomeria-10-questoes-561990.shtml Acesso em: 22. set. 2010.
Disponível em: http://pt.wikipedia.org/wiki/Isomeria_plana Acesso em: 22. set. 2010.
Disponível em: http://www.algosobre.com.br/quimica/isomeria.html Acesso em: 22. set. 2010.
Disponível em: http://www.coladaweb.com/quimica/quimica-inorganica/isomeria Acesso em: 22. set. 2010.
Disponível em: http://www.mundoeducacao.com.br/quimica/historia-da-isomeria.htm Acesso em: 22. set. 2010.
Disponível em: http://www.mundoeducacao.com.br/quimica/isomeros.htm Acesso em: 22. set. 2010.
Disponível em: http://www.mundovestibular.com.br/articles/77/1/ISOMERIA-/Paacutegina1.html Acesso em: 22. set. 2010.
Equipe 2. Pesquisar sobre os descobridores do fenômeno, fazendo um levantamento de suas vidas e em que outras áreas da química (ou ciências naturais em geral) tiveram participação marcante.
Disponível em: http://www.dec.ufcg.edu.br/biografias/JonsBerz.html Acesso em: 22. set. 2010.
Disponível em: http://www.portalsaofrancisco.com.br/alfa/berzelius-jons-jacob/bernzelius-jons-jacob.php Acesso em: 22. set. 2010.
Equipe 3. Criar um roteiro de uma simulação artística (teatro, desenho, quadrinhos, filme) desta história inicial do conceito químico de isomeria. Há um tutorial para criar roteiros:
Disponível em: http://www.massarani.com.br/Roteiro.html Acesso em: 22. set. 2010.
Equipe 4. Realizar a produção artística, seja em qualquer meio, citado ou não citado na etapa anterior.
Equipe 5. Construir uma "linha do tempo" para o conceito de isomeria, partindo da descoberta até as aplicações atuais do fenômeno. Não esquecer de falar um pouco sobre os cientistas relacionados as descobertas.
Há um tutorial para construir a linha do tempo disponível em: http://julianagsouzadias.blogspot.com/2010/04/dicas-para-criar-uma-linha-do-tempo.html Acesso em: 22. set. 2010.
Para efetuar leituras e desenvolver as atividades os alunos devem acessar a Webquest (Metodologia de pesquisa online, orientada por um roteiro com os seguintes passos: introdução, tarefa, recursos, processo, avaliação, conclusão.) que está disponível em:
http://www.webquestbrasil.org/criador/webquest/soporte_tablon_w.php?id_actividad=5729&id_pagina=1 Acesso em: 22. set. 2010.
Atividade 3
Esta atividade tem como objetivo levar o aluno a pesquisar as características dos elementos Etano, Metano, Propano e Butano. A pesquisa pode ser realizada na sala de aula, na biblioteca, em casa ou no laboratório de informática. Os alunos devem ser organizados em equipes compostas por cinco pessoas. Cada equipe deve buscar informações como: quantidade de átomos, cor, cheiro, produção industrial, solubilidade, teor inflamável, tipo de gás, uso e aplicação no cotidiano. Para apresentar os resultados cada equipe deve criar a apresentação.
Catarse
A catarse pode ser desenvolvida no laboratório de informática (se os alunos forem utilizar o recurso Cmap) ou na sala de aula (se forem utilizar a cartolina). Os alunos devem se organizar em equipes formadas por 4 pessoas. Cada equipe cria seu mapa conceitual para representar os estudos sobre Isomeria. Mapas Conceituais são representações gráficas semelhantes a diagramas, que indicam relações entre conceitos ligados por palavras. Representam uma estrutura que vai desde os conceitos mais abrangentes até os menos inclusivos. São utilizados para auxiliar a ordenação e a sequenciação hierarquizada dos conteúdos de ensino, de forma a oferecer estímulos adequados ao aluno.
Para saber mais sobre Mapas conceituais você pode acessar o endereço: http://cmaptools.softonic.com.br/ Acesso em: 22. set. 2010.
Caso não tenha acesso ao Cmap, pode-se construir os mapas utilizando cartolina. No link abaixo há um exemplo que pode auxiliar no desenvolvimento da atividade.
Link: http://cmapspublic.ihmc.us/rid=1164653387734_251334531_6356/Mapa%20conceitual%20de%20isomeria.cmap Acesso em: 22. set. 2010.
Os alunos podem se organizar na sala de aula, em equipes constituidas por quatro pessoas e criar painéis utilizando imagens e fotografias para representar a Isomeria. Como exemplo, sugerimos imagens de pessoas gêmeas, etc. Após concluírem podem afixar no mural da escola.
Matemática: os alunos podem desenvolver a construção do Tangram posteriormente, montar figuras de maneira a compreender o que é Isomeria.
Artes: os alunos podem criar o Tangram utilizando materiais diferentes entre eles: cartolina, cerâmica, papelão, etc.
Biologia: o professor pode trabalho os efeitos da Glicose e Frutose no organismo humano.
Ciências: o professor pode trabalhar sobre a quantidade diária necessária de Glicose e Frutose para o corpo humano.
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Metano | Imagem |
| Propano | Imagem |
| Butano | Imagem |
| Etano (eclipsado) | Imagem |
Recursos Complementares
Livro: NEHMI, Victor A. Química. São Paulo: Ática. 1995.
Link para acessar o site do Ludo Químico: Disponível em: http://www.ludoquimico.com.br/ Acesso em: 22. set. 2010.
Tutorial (livro) da TV Pendrive disponível em: http://www.diaadia.pr.gov.br/multimeios/arquivos/File/livro/livro.html Acesso em: 22. set. 2010.
Avaliação
O processo de avaliação deve ser formativo, processual e diagnóstico. Sugerimos alguns critérios pelos quais o professor pode avaliar se: relataram a produção textual sobre as origens do conceito químico de isomeria de acordo com as normas da Língua Portuguesa; pesquisaram sobre a vida e obra dos teóricos fundamentados nos parâmetros da metodologia da pesquisa científica; utilizaram recursos adequadamente para criar a linha do tempo dos conhecimentos em Isomeria e desenvolveram a produção artística com criatividade.
Sem estrelas 0 classificações
- Cinco estrelas 0/0 - 0%
- Quatro estrelas 0/0 - 0%
- Três estrelas 0/0 - 0%
- Duas estrelas 0/0 - 0%
- Uma estrela 0/0 - 0%
Denuncie opiniões ou materiais indevidos!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus







 Etano (eclipsado)
Etano (eclipsado)