27/09/2010
Suelen Fernanda Machado
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
| Ensino Médio | Química | Transformações: caracterização, aspectos energéticos, aspectos dinâmicos |
| Ensino Médio | Física | Calor, ambiente e usos de energia |
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
| Ensino Médio | História | Memória |
| Ensino Médio | Língua Portuguesa | Gêneros discursivos e textuais: narrativo, argumentativo, descritivo, injuntivo, dialogal |
O que o aluno poderá aprender com esta aula
- Conhecer o conceito de cinética química.
- Reconhecer a cinética química no cotidiano.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Os alunos devem ter conhecimento sobre reações químicas.
Estratégias e recursos da aula
Prática social inicial do conteúdo
Na sala de aula pergunte aos alunos: Porque nem toda reação química acontece no mesmo tempo? Após dialogarem entre si.Explique que as reações químicas ocorrem em velocidades diferentes (ex: o processo de digestão dos alimentos e a queima de uma vela, que levam algumas horas e uma explosão e a queima de um palito de fósforo, que levam alguns segundos, formação da ferrugem, que levam anos para se formar; dissolução de uma pastilha efervescente, que levam alguns segundos; decaimento radioativos, que levam muitas vezes bilhões de anos; formação das rochas, que levam alguns milhões de anos, etc.) devido a fatores como: temperatura, superfície de contato, pressão, concentração, presença de luz, catalisador e inibidores
Fonte: http://www.soq.com.br/conteudos/em/cineticaquimica/p5.php
Problematização
Que fatores influenciam na velocidade das reações químicas?
Instrumentalização
A cinética química é a ciência encarregada de estudar a velocidade das reações químicas de processos químicos bem como os fatores que as influenciam.
Explique aos alunos que por vezes é necessário e importante fazer o controle das reações, seja para acelerar ou retardar o processo. Dentre os fatores que influenciam na velocidade das reações químicas estão: o estado físico dos reagentes, a concentração dos reagentes, a temperatura em que a reação ocorre, e se ou não, algum catalisador está presente na reação.
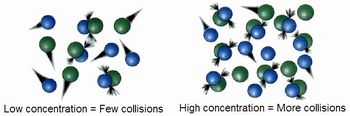
Professor explique aos alunos que ao se analisar a imagem se pode observar que em baixa concentração (Low concentration = Few collisions) há poucas colisões. Em alta concentração (High concentration = More collisions) há mais colisões.
Fonte: http://upload.wikimedia.org/wikipedia/commons/4/41/Molecular-collisions.jpg
Em 1864, Peter Waage e Cato Guldberg, os pioneiros no desenvolvimento da cinética química formularam, a Lei de Ação das Massas.
Fonte: http://pt.wikipedia.org/wiki/Ficheiro:Guldberg_Waage.jpg
Para complementar os estudos, encaminhe os alunos ao laboratório de informática. Peça que acessem o recurso e respondam as questões conforme o roteiro disponível no recurso.
Link: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=22024
Atividade 1
Esta atividade tem como objetivo pesquisar sobre os teóricos que contribuíram para com a cinética química consequentemente conhecer o conceito de cinética química. Desta maneira, os alunos devem ser organizados em duplas para desenvolver a atividade. Roteiro: Os alunos devem pesquisar em livros em casa ou nas bibliotecas e ou sites sobre a vida e obra de Cato Maximilian Guldberg e Peter Waage. Devem ser coletados os seguintes dados: data de nascimento e morte, nacionalidade, formação acadêmica, área de pesquisas, teorias, etc. Após finalizar a atividade os alunos devem criar um blog e disponibilizar as informações.
Blog: É um espaço gratuito, interativo, online, para dialogar com seus colegas, com a comunidade, onde o autor pode inserir textos, imagens, vídeos, áudios, etc. Para criar o blog eles devem acessar o link: https://www.blogger.com/start
Há um tutorial disponível no link abaixo o qual é possível buscar informações para criar o blog.
Link: http://portaldoprofessor.mec.gov.br/storage/materiais/0000013567.pdf
Link´s para pesquisa:
- http://www.netsaber.com.br/biografias/ver_biografia_c_1792.html
- http://www.dec.ufcg.edu.br/biografias/CatoMaxi.html
- http://pt.wikilingue.com/es/Peter_Waage
- http://www.infopedia.pt/$cato-guldberg
Atividade 2
Professor, sugerimos que utilize o endereço http://www.webquestbrasil.org e construa uma Webquest, sobre a Lei de Guldberg-Waage (Lei de Ação das Massas) e sobre a citação “A velocidade de uma reação é diretamente proporcional ao produto das concentrações molares dos reagentes, quando estes estão elevados a expoentes, que são os seus respectivos coeficientes estequiométricos”. Após construir a Webquest, reúna os alunos e forme equipes em que estejam presentes três pessoas. Solicite que pesquisem no seu recurso de acordo com o roteiro. Roteiro: Os alunos devem acessar a Webquest, pesquisar em livros e ou em sites, desenvolver as atividades incluir alguns exemplos no sentido de reconhecer a cinética química no cotidiano. Para contribuir na sua produção, disponibilizamos os sites abaixo:
- http://www.colegioweb.com.br/quimica/lei-de-guldbergwaage-lei-da-acao-das-massas
- http://www.sofi.com.br/node/762
- http://www.scribd.com/doc/3219898/Quimica-Cinetica-Quimica-Lei-de-Guldberg-e-Waage-ou-lei-da-Acao-das-Massas
Atividade 3
Esta atividade tem como objetivo levar o aluno conhecer o conceito de cinética química e reconhecer a cinética química no cotidiano. Roteiro: os alunos devem copiar a questão no caderno, responder e efetuar a correção em sala de aula. Peça aos alunos que resolvam a questão assinalando com um x a alternativa correta.
(OSEC) Em uma reação, o complexo ativado:
a) ( ) Possui mais energia que os reagentes ou os produtos.
b) ( ) Age como catalisador.
c) ( ) Sempre forma produtos.
d) ( ) É composto estável.
e) ( ) Possui menos energia que os reagentes ou os produtos.
Resposta: os alunos devem assinalar a questão a.
Catarse
Organize os alunos em equipes formadas por três pessoas cada uma. Solicite que utilizem o Laboratório de Informática retomem os conteúdos trabalhados nas Atividades 1, 2 e 3 para pesquisar e construir um mapa conceitual com os conteúdos abordados nesta aula. Esta ação deve evidenciar a compreensão dos conteúdos trabalhados. Professor se houver alunos que não se apropriaram de algum conteúdo, proponha que retomem aos recursos utilizados. Roteiro: Após criarem os mapas cada equipe deve se organizar na sala de aula, fazer a projeção e explicar o mapa que criaram. Desta maneira podem analisar as várias possibilidades de construção dos mesmos. Para criar o mapa conceitual os alunos podem utilizar o programa Cmap Tools que está disponível no endereço: http://penta2.ufrgs.br/edutools/mapasconceituais/
Para saber mais sobre mapas conceituais basta acessar o link: http://cmaptools.softonic.com.br/
Interdisciplinaridade
- Física: a partir desta aula os alunos podem estudar sobre energia cinética.
- História: os alunos podem pesquisar sobre a História da Cinética Química.
- Língua Portuguesa: nesta disciplina os alunos podem produzir textos que contenham as teorias criadas por químicos que se envolveram com a cinética química.
Prática social final dos conteúdos
Proponha aos alunos que utilizem o mural do estabelecimento para afixar os mapas conceituais. No decorrer da semana cada equipe pode explicar a outras turmas como e porquê construíram tais recursos.
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Cinética química | Software Educacional |
Recursos Complementares
Link: http://pt.wikipedia.org/wiki/Cin%C3%A9tica_qu%C3%ADmica
Link: http://dicasdequimica.vilabol.uol.com.br/cinetica.html
Link´s http://www.soq.com.br/conteudos/em/cineticaquimica/
Os alunos podem pesquisar sobre a História da Cinética Química no site:
Link: http://www.marco.eng.br/cinetica/trabalhodealunos/CineticaBasica/historia.html
Avaliação
Professor tornamos disponíveis alguns critérios para que possa desenvolver a avaliação.
- Relataram detalhadamente as informações acerca da vida e obra dos teóricos;
- Pesquisaram a Lei das Massas e incluíram todos dados solicitados no blog;
- Participaram cooperativamente para a realização das tarefas em equipe;
- Manusearam e exploraram corretamente todos os recursos tecnológicos;
- Elaboraram a atividade escrita de acordo com as regras da Língua Portuguesa ao pesquisar na Webquest.
Sem estrelas 0 classificações
- Cinco estrelas 0/0 - 0%
- Quatro estrelas 0/0 - 0%
- Três estrelas 0/0 - 0%
- Duas estrelas 0/0 - 0%
- Uma estrela 0/0 - 0%
Denuncie opiniões ou materiais indevidos!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus




 Cinética química
Cinética química