15/10/2010
Cláudia Regina Montes Gumerato
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Educação de Jovens e Adultos - 2º ciclo | Ciências Naturais | Terra como espaço para a vida |
| Ensino Fundamental Final | Ciências Naturais | Vida e ambiente |
| Ensino Fundamental Final | Ciências Naturais | Tecnologia e sociedade |
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
O que o aluno poderá aprender com esta aula
Reconhecer a presença de misturas homogêneas no cotidiano.
Classificar a tinta de caneta como uma mistura homogênea.
Identificar os componentes da tinta de caneta a partir da aplicação de processos de separação de misturas a esse material.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Conceito de matéria.
Propriedades gerais e específicas da matéria;
Conceito de mistura e distinção entre as misturas homogêneas e heterogêneas.
Estratégias e recursos da aula
Professor, a primeira aula foi planejada para ser executada em um laboratório de química/ciências, ou espaço similar (até mesmo em sala de aula, se não houver esse espaço na escola), onde os alunos deverão ser divididos em grupos de, no máximo, cinco alunos. Ao longo da descrição da aula serão apresentados o desenvolvimento e discussão da mesma. No início dessa aula, cada aluno deverá ter em mãos uma do roteiro previamente digitado com as intruções e espaços para anotações. Na segunda aula, os alunos deverão ser encaminhados ao laboratório de informática a fim de realizarem pesquisa para uma ampliação dos conhecimentos teóricos sobre a cromatografia e sua utilização como processo de separação de misturas homogêneas. Na terceira aula, cada grupo de alunos produzirá um relatório no qual deverão convergir os conhecimentos advindos da pesquisa teórica e da atividade experimental.
Aula 1- Separação dos componentes de misturas homogêneas
Professor, para o início dessa aula disponibilize em uma bancada do laboratório diferentes tipos de substâncias que fazem parte do cotidiano dos alunos, tais como: café coado; leite; maionese e tintas de canetas. Retome com seus alunos os conceitos de substâncias puras e misturas já trabalhados, indagando-os a respeito das substâncias apresentadas. Discuta com eles a classificação dessas substâncias enquanto misturas homogêneas e levante hipóteses a respeito dos processos que poderiam ser utilizados para a separação dos seus componentes.
Em seguida, separe-os em grupos de, no máximo, cinco alunos e encaminhe cada grupo para sua bancada onde realizarão a atividade experimental proposta.
As imagens e parte do conteúdo dessa aula estão disponíveis no endereço: http://www.invivo.fiocruz.br/cgi/cgilua.exe/sys/start.htm?infoid=989&sid=3
Acessado em 15/09/2010.
Material
6 tiras de papel (de preferência aquele papel dos filtros de café);
2 copinhos plásticos;
Um pouco de água;
Um pouco de álcool (Cuidado: mantenha o álcool longe do fogo!);
Canetas (hidrocor) nas cores amarelo, azul claro, rosa e outra cor de sua preferência.
Agora siga as instruções e vá anotando suas observações.
Parte 1 – Corrida de cores
Conte a medida de um dedo do fundo dos copos para cima e faça uma marca.
Em seguida, em um deles, coloque álcool e no outro, água.
Atenção: o líquido deve estar na altura da marca no copo ou abaixo.
Pegue duas tiras de papel. Em cada uma delas, marque três pontos: um na cor rosa, um em amarelo e outro em azul claro.
Os pontos devem ser desenhados a um dedo da extremidade do papel.
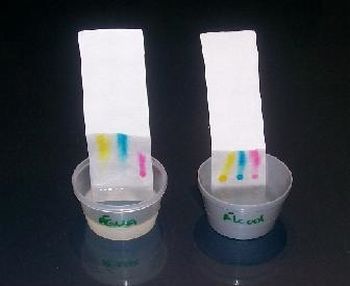
Mergulhe uma tira no copo com água e outra no copo com álcool, com a extremidade do papel mais próxima do desenho voltada para baixo. Os pontos desenhados não devem ficar imersos no líquido, mas um pouco acima.
Aguarde e observe. Registre as suas observações e discuta-as com seus colegas de grupo.
Qual a cor sobe mais rápido no álcool?
Qual a cor sobe mais rápido na água?
Por que uma cor sobe mais rápido que a outra?
Parte 2 – Mistura de cores primárias
Agora separe mais três tiras de papel. Na primeira você vai desenhar um risco (na mesma altura que desenhou os pontinhos da primeira parte) usando primeiro a caneta amarela e por cima a azul clara. Na segunda vai fazer o mesmo desenho usando as canetas amarela e rosa. E na terceira vai usar as canetas azul claro e rosa.
Verifique a cor que foi formada em cada tira a partir das misturas. Para não esquecer quais são essas novas cores, anote-as.
Coloque a primeira tira apenas na água (Não deixe o risco encostar no líquido!).
Aguarde e observe.
O que aconteceu?
Em seguida repita a mesma operação na água com as outras duas tiras.
Observe cada uma. Qual a cor resultante da mistura do amarelo com o azul claro? E do amarelo com o rosa? E do azul claro com o rosa?
Parte 3 – Usando outras cores
Agora escolha outra cor de sua preferência e faça o risco na tira de papel.
No nosso caso escolhemos preto. Ponha a tira no copinho com água.
Aguarde e observe. Se quiser, repita com outras cores.
Então, houve aparecimento de outras cores? Como você explica o que aconteceu
O que você acha que aconteceria se nas duas últimas partes da experiência usássemos álcool no lugar de água?
Quer saber? Experimente e anote suas observações.
Parte 4- Analisando as tintas de canetas esferógráficas.
Agora você deverá realizar os mesmos procedimentos anteriores usando canetas esferográficas - aquelas que utiliza diariamente em seus registros escolares - de três cores diferentes, incluindo a preta. Faça os traços no papel de filtro e mergulhe o papel no álcool e na água (sem encostar a tinta nos líquidos). Obsereve os resultados anotando-os para a discussão.
Discussão em grupo
Os resultados no álcool e na água são iguais? Como vocês explicam esse fato?
Quais são os resultados para cada cor? Como vocês explicam esses resultados?
A tintas de canetas esferográficas são substâncias puras ou misturas? Em que você se baseou para responder?
Quantos componentes puderam ser identificados na tinta de caneta preta?
Qual dos componentes da tinta de caneta preta é mais solúvel em álcool?
Entendendo o que aconteceu
Professor, ao fechar essa discussão com seus alunos, possibilite que cada grupo de alunos exponha suas discussões. Em seguida, destaque aspectos referentes à solubilidade de cada tipo de tinta (hidrográfica e esferográfica) em álcool e em água, assim como a composição de cada tipo de tinta e de cor, quanto aos pigmentos que as compõem.
Partes 1, 2 e 3- À medida em que a água sobe pelo papel, a tinta é dissolvida e se espalha. As cores escalam o papel – algumas avançando mais rápido que as outras. Isso acontece porque as fibras de celulose do papel interagem com a água e os pigmentos. Os corantes das canetinhas têm composição química diferente, e é o tipo de interação do corante com o papel que irá determinar o quanto ele subirá. Quanto mais forte for a interação, mais lento será o processo.
Parte 4- Quando o papel de filtro é mergulhado no álcool, este líquido começa a subir molhando o papel e arrastando os componentes da tinta que são solúveis em álcool. Cada componente é arrastado com uma velocidade diferente ocorrendo, assim, a separação.
Chamamos este processo de separação de substâncias de cromatografia e ele é usado de diversas formas para se separar e identificar substâncias químicas, mesmo em misturas complexas contendo centenas de compostos.
Aula 2 - Cromatografia
Professor, inicie essa aula retomando as observações e discussões ocorridas na aula anterior. Em seguida forme grupos de no máximo três alunos, para que possam efetuar uma pesquisa na internet. Para isso deverão acessar preferencialmente os sites indicados, que deverão ser apresentados a eles no início da aula, por meio de um pequeno roteiro.
Na página http://www.explicatorium.com/CFQ7-Cromatografia.php (acessado em 15/09/2010) os alunos deverão primeiramente assistir ao vídeo sobre a cromatografia em papel disponível no final da página.
Após assitirem ao védeo, os alunos deverão ler todo o texto, discutir as informações e, em seguida, registrar:
Quem descobriu essa técnica e em que circunstâncias isso aconteceu.
Em que consiste esse processo de separação de misturas.
No endereço http://pt.wikipedia.org/wiki/Caneta_esferogr%C3%A1fica (acessado em 15/09/2010) é feito uma abordagem histórica sobre a invenção da canta esferográfica. Sugerimos a sua leitura e anotações de informações que os alunos considerarem amis interessantes. Chama a atenção no texto as questões políticas e econômicas envolvidas no desenvolvimento desse objeto atualmente tão necessário e popular.
Possibilidade de interdisciplinaridade
O professor de Ciências Naturais/Química poderá planejar com o de História um momento de discussão desses aspectos históricos da invenção e desenvolvimento da caneta esferográfica.
Ao final dessa aula, o professor deverá possibilitar aos alunos a exposição de seus registros e discutir as questões apresentadas, fazendo os esclarecimentos que se fizerem necessários.
Aula 3- Produção de relatórios em grupos
Nessa aula deverão ser formados os mesmos grupos de alunos que fizeram juntos as atividades no laboratório de Ciências/química na primeira aula, para que produzam o relatório em grupo, dos estudos sobre o tema desenvolvido nas duas aulas anteriores.
Roteiro para elaboração do relatório da atividade experimental
TÍTULO: Frase sucinta que indica o principal objetivo da experiência.
RESUMO: Texto de no máximo cinco linhas descrevendo tudo o que foi feito, inclusive os resultados alcançados.
INTRODUÇÃO: Descrição da teoria necessária ao entendimento da prática e da discussão dos resultados. Deve ser uma síntese das fontes consultadas. Ao final da introdução, como último parágrafo, vem o objetivo do trabalho.
PROCEDIMENTO EXPERIMENTAL: Descrever o procedimento experimental, ressaltando os principais materiais e equipamentos utilizados.
RESULTADOS: Consiste na apresentação de todos os dados colhidos em laboratório ou dos calculados decorrentes dos dados. Podem ser apresentados na forma de tabelas, gráficos, etc., se isso melhorar a comunicação dos dados.
RESULTADOS E DISCUSSÃO: Discutir os dados obtidos à luz da teoria exposta. Geralmente as questões para a discussão estão apontadas no roteiro da aula.
CONCLUSÃO: Síntese pessoal sobre as conclusões alcançadas com o seu trabalho. Enumere os resultados mais significativos do trabalho. Não deve apresentar nenhuma conclusão que não seja fruto da discussão.
REFERÊNCIAS: Livros, textos e sites usados para escrever o relatório, devem ser citados
Recursos Complementares
http://qnesc.sbq.org.br/online/qnesc07/atual.pdf . Acessado em 16/08/2010.
http://qnesc.sbq.org.br/online/qnesc07/exper3.pdf Acessado em15/09/2010.
http://www.feiradeciencias.com.br/sala21/21_11.asp Acessado em 16/09/2010.
Análise de Pigmentos de Pimentões por Cromatografia em Papel. Disponível em http://qnesc.sbq.org.br/online/qnesc29/08-EEQ-0707.pdf . Acessado em 15/09/2010.
AMBROGI, A e LISBÔA, J.C.F. Misturas e substâncias: reações químicas. SãoPaulo: Editora Hamburg, 1983.
Avaliação
A avaliação do conteúdo deverá ser realizada de maneira processual, ao longo das aulas e de cada atividade desenvolvida.
Poderão ser utilizados como instrumentos avaliativos os registros, a pesquisa, as discussões e a participação individual e coletiva na socialização.
Deverá ser usado como instrumento principal de avaliação quantitativa o relatório da atividade experimental contendo pesquisas teóricas oriundas do próprio referencial utilizado nas aulas.
Quatro estrelas 2 classificações
- Cinco estrelas 1/2 - 50%
- Quatro estrelas 0/2 - 0%
- Três estrelas 1/2 - 50%
- Duas estrelas 0/2 - 0%
- Uma estrela 0/2 - 0%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
Calebe, aafsgdfgafa , Goiás - disse:
skateboardlifestyle@hotmail.com12/11/2012
Três estrelasMais quem inventou ou descobriu a separação de misturas?
-
Luciana, Escola Estadualm Profa Olga Barreto , Sergipe - disse:
lubiologa@gmail.com19/10/2010
Cinco estrelasUma ótima oportunidade de fazer uma aula dinâmica com baixo custo!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus