14/01/2011
Eziquiel Menta
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Física | Calor, ambiente e usos de energia |
O que o aluno poderá aprender com esta aula
Distinguir transformações isotérmicas, isobáricas e isovolumétricas;
Interpretar gráficos de transformações gasosas.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Conceito de pressão e temperatura;
Definição de quantidade de matéria;
Lei Geral dos Gases Perfeitos.
Estratégias e recursos da aula
Estratégias de ensino:
- Aula interativa com recursos multimeios;
- Aula conceitual.
Materiais:
Atividade 1:
- uma mamadeira graduada;
- uma seringa de injeção nova e grande (com agulha);
- uma borracha de apagar (preferencialmente de formato retangular);
- papel milimetrado.
Atividade 2:
- rabo quente;
- termômetro;
- seringa de injeção nova e grande (pode ser a mesma da atividade 1);
- super bonder.
- panela com água
Introdução à aula:
Pergunte aos alunos se eles já perceberam que imediatamente após fechar a porta de geladeira fica mais difícil abri-la ou que um frasco de desodorante se resfria ao liberar o spray. Comente que estas situações poderão ser explicadas através dos estudos das transformações gasosas. Para isso, será necessário definir as grandezas envolvidas em cada transformação bem como quais variam em cada processo. Explique que dependendo da grandeza que permanecer constate, a transformação receberá um nome específico.
Figura 1: Geladeira
Disponível em: http://futebolveteranos.zip.net/images/geladeira.jpg acesso em 15/11/2010.
Atividade 1 - Laboratório experimental: Transformação isotérmica
Esta atividade tem como objetivo realizar uma experiência variando a pressão e o volume mas, mantendo a temperatura constante. Ao final da atividade você poderá apresentar a Lei de Boyle-Mariotte e sortear um dos grupos para apresentar os dados obtidos realizando uma exposição dos dados e das técnicas experimentais desenvolvidas por cada um dos grupos.
Peça aos alunos que tragam para aula os materiais necessários para a realização da experiência. Separa os alunos em grupos de 3 ou 4 pessoas e peça para que sigam o roteiro proposto.
ROTEIRO PROPOSTO:
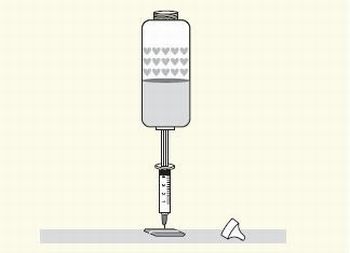
Figura 2: Montagem da atividade experimental - Transformação Isotérmica
Desenho retirado do material didático do 2º ano do EM da rede CNEC
1º) Monte a seringa com a agulha e puxe o embola obtendo o maior volume possível;
2º) Espete a agulha na borracha e vede a saída de ar;
3º) Monte uma tabela como a do exemplo:
| Volume de água na mamadeira (ml) |
Massa de água na mamadeira (g) |
Força peso da água (N) |
Variação da pressão na seringa (Pa) |
Variação do volume na seringa (m3) |
Produto da variação da pressão pela variação do volume na seringa |
| 0 |
|
|
|
|
|
| 50 |
|
|
|
|
|
| 100 |
|
|
|
|
|
| 150 |
|
|
|
|
|
| 200 |
|
|
|
|
|
| 250 |
|
|
|
|
|
| 300 |
|
|
|
|
|
3º) Coloque a mamadeira em cima do embolo e anote como 0 a "Massa de água na mamadeira". Perceba que quando a mamadeira está vazia este volume corresponde à pressão atmosférica visto que a mamadeira está submetida apenas pressão atmosférica;
4º) Adicione, por vez, 50 ml de água anotando na tabela o volume de gás dentro da seringa (penúltima coluna da tabela). Lembre-se que na seringa a graduação volumétrica é marcada em ml (1ml = 1 cm3). Faça a conversão antes de anotar os valores na última coluna da tabela.
5º) Determine a massa de água dentro da mamadeira sabendo 1ml = 1 g;
6º) Determine o peso de água sabendo que 1 N corresponde ao peso de 100 g;
7º) Para determinar a variação da pressão sobre o gás é necessário saber a área da secção transversal interna de seringa (Área = pi . raio ao quadrado). Ao dividir a força aplicada pelo gás (terceira coluna) pela área tem-se a variação da pressão sobre o gás.
8º) Construa um gráfico da variação da pressão na seringa (Pa) em função da variação do volume no gás (m3).
ANÁLISE DOS DADOS
Peça para os alunos multiplicarem a variação da pressão pela variação do volume na seringa anotando na tabela 1. O produto obtido deverá ser constante. Desta forma podemos concluir que P1V1 = P2V2 = P3V3 = constante.
Explique para os alunos que este fenômeno segue a Lei de Boyle-Mariotte na qual em temperatura constante a variação da pressão é inversamente proporcional a variação do volume.
Atividade 2 - Laboratório experimental: Transformação isobárica
Esta atividade tem como objetivo realizar uma experiência variando a temperatura e o volume mas mantendo a pressão constante. Para evitar acidentes, e preferível que você, professor, faça o experimento demonstrativamente realizando, por si, os procedimentos experimentais. Ao final da atividade será possível enunciar a Primeira Lei de Charles e Gay-Lussac. Os alunos irão acompanhar os procedimentos experimentais anotando os valores na tabela e realizando as conclusões.
ROTEIRO PROPOSTO:
1º) Puxe o embolo até a metade da seringa (preferencialmente em uma demarcação exata da graduação volumétrica);
2º) Lacre a ponta da agulha da seringa com duas ou três gotas da cola de super bonder;
3º) Monte uma tabela como a do exemplo:
| Temperatura (K) |
Volume (ml) |
Variação do volume (ml) |
Razão entre variação do volume pela temperatura |
| Ta |
|
|
|
| Ta + 20 |
|
|
|
| Ta + 40 |
|
|
|
| Ta + 60 |
|
|
|
4°) Submersa a seringa dentro da água em temperatura ambiente (será necessário algum peso para manter a seringa submersa e meça com o termômetro) e anote seu volume inicial. Coloque o termômetro dentro da água e meça a temperatura ambiente (Ta) da água e transforme-a para Kelvin;
5º) Submersa o rabo quente na água e ligue-o;
6º) A cada variação de 20°C na temperatura meça o volume de gás dentro da seringa, até completar a coluna 1 da tabela 2;
7º) Calcule a variação do volume e a razão entre esta variação do volume e a variação da temperatura. Anotar estes valores na tabela 2.
ANALISE DOS DADOS:
Deixa claro para os alunos que a razão entre o volume pela temperatura é constante: V1/T1 = V2/T2 = V3/T3 = constante.
Explique para os alunos que este fenômeno segue a Primeira Lei de Charles e Gay-Lussac na qual em pressão constante a variação do volume é diretamente proporcional a variação da temperatura
Atividade 3 - Laboratório de informática: Transformação isocórica, isométrica ou isovolumétrica
Esta atividade terá como objetivo compreender, por meio de uso de um simulador, a relação entre as grandezas temperatura e pressão em transformações isocóricas. Ela será realizada no laboratório de informática vista as dificuldades de montagem e obtenção dos dados experimentais.
Ao final da atividade você poderá apresentar a Segunda Lei de Charles e Gay-Lussac e sortear um dos grupos para apresentar os dados obtidos. É importante que seja realizada uma discussão sobre os dados para tirar possíveis dúvidas dos alunos.
Separe os alunos em duplas, disponibilize o recurso 1 e entregue o roteiro proposto.
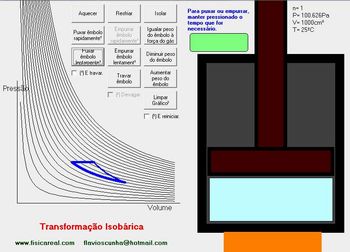
Recurso 1: Transformações gasosas
Disponível em: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=11277 acesso em 15/11/2010.
ROTEIRO PROPOSTO:
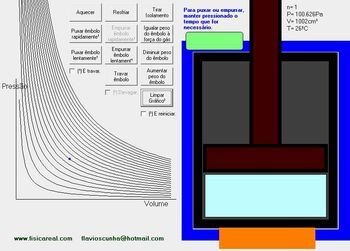
1º) Com o simulador aberto, escolha um volume que será mantido constante durante a simulação (sugestão: entre 1000 a 1002 cm3).
Figura 3: Volume de 1002 cm3
Disponível em: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=11277 acesso em 15/11/2010.
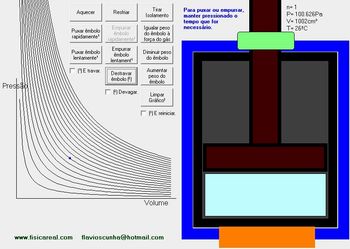
2º) Clique em "Travar em êmbolo" para que o volume mantenha-se com o valor escolhido;
Figura 4: Êmbolo travado
Disponível em: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=11277 acesso em 15/11/2010.
3º) Monte uma tabela como a do exemplo:
| Temperatura (K) |
Pressão (Pa) |
Razão entre temperatura e pressão |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
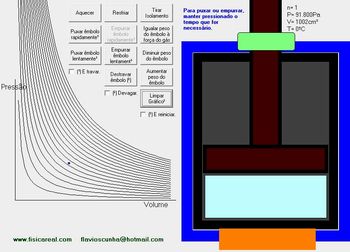
4°) Para iniciar a coleta de dados, sugerimos que primeiro atinja a temperatura de 0°C, transforme-a para a para o sistema internacional (K) e anote na tabela. Para isso, clique em aquecimento ou resfriamento até obter a temperatura de 0°C.
Figura 5: Temperatura de 0°C
Disponível em: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=11277 acesso em 15/11/2010.
5°) Clique em "Limpar gráfico" para obter um gráfico da situação que será estudada.
6º) Agora clique em "Aquecer" e recolha valores de temperatura e pressão para preencher a tabela.
7º) Realize a razão entre os valores obtidos e completa a última coluna da tabela.
ANALISE DOS DADOS:
O que foi possível concluir analisando o quociente da razão entre temperatura e pressão? (Resposta sugerida: sempre será um valor constante)
Qual o formato do gráfico: "Pressão x Volume" apresentado pelo simulador? (Resposta sugerida: uma reta paralela ao eixo y)
Qual o nome da transformação ocorrida e apresentada pelo simulador? (Resposta sugerida: Transformação Isovolumétrica)
Discuta com seus colegas, como seria possível obter uma transformação isobárica ou uma transformação isotérmica? (Resposta sugerida: Para uma transformação isobárica basta destravar o êmbolo e aquecer ou resfriar o gás. Já para uma transformação isotérmica é necessário tirar o isolamento térmico, esperar o sistema atingir o equilíbrio térmico e puxar ou empurrar lentamente o êmbolo).
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Transformações gasosas | Animação/simulação |
Recursos Complementares
Lista de exercícios sobre "Transformações gasosas" - http://www.portalimpacto.com.br/docs/Aula18Ewerton2AnoF3.pdf acesso em 15/11/2010.
Material do GREF sobre transformações gasosas - http://www.if.usp.br/gref/termo/termo3.pdf acesso em 15/11/2010.
Informações sobre transformações gasosas - http://www.scribd.com/doc/42268168/Transformacoes-gasosas acesso em 15/11/2010.
Avaliação
Os alunos serão avaliados através da participação nas aulas, nas apresentações das atividades desenvolvidas, na entrega dos gráficos das atividades 1 e 2 e nas analises das atividades 1, 2 e 3.
Quatro estrelas 1 classificações
- Cinco estrelas 0/1 - 0%
- Quatro estrelas 1/1 - 100%
- Três estrelas 0/1 - 0%
- Duas estrelas 0/1 - 0%
- Uma estrela 0/1 - 0%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
Ana Cláudia, Fundação Bradesco , Rio Grande do Norte - disse:
delgadoana1@hotmail.com16/02/2012
Quatro estrelasEsta aula realmente é muito interessante,pois permite o aluno visualisar na prática a teoria estudada.
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus



 Transformações gasosas
Transformações gasosas