29/08/2008
Wildson Luiz Pereira dos Santos
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Transformações: caracterização, aspectos energéticos, aspectos dinâmicos |
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
O que o aluno poderá aprender com esta aula
• Determinar o vetor de momento de dipolo resultante de uma molécula;
• Determinar a polaridade das moléculas a partir dos vetores de momento de dipolo.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
• Geometria molecular;
• Soma vetorial.
Estratégias e recursos da aula
Conteúdos específicos:
• Vetor de momento de dipolo elétrico;
• Polaridade das moléculas;
• Eletronegatividade.
Recursos educacionais:
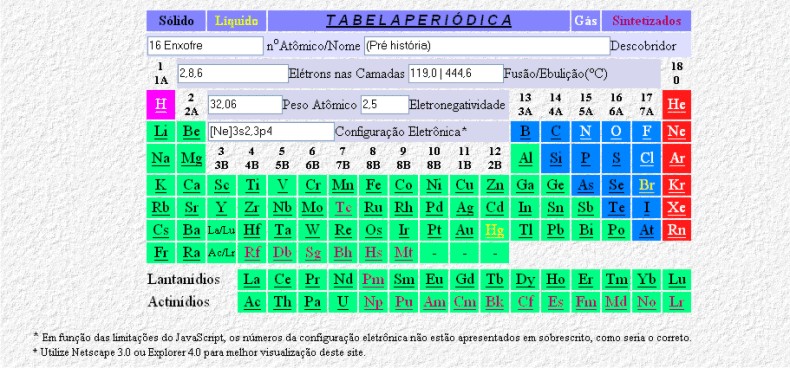
• Tabela periódica: www.cdcc.sc.usp.br/quimica/tabelaperiodica/tabelaperiodica1.htm;
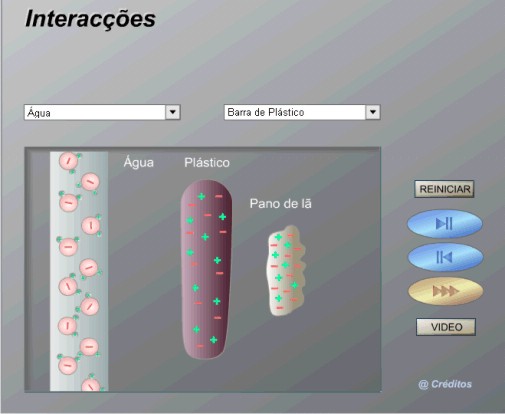
• Simulações e vídeos sobre a polaridade da água e de outras substâncias: nautilus.fis.uc.pt/cec/molecularium/pt/ligintermol/interaccoes/index.html.
Preparando a aula:
Na aula anterior, informe aos alunos que a próxima aula será no laboratório de informática.
Introduzindo a aula: (5 min.)
Inicie a aula perguntando aos alunos se algum líquido pode ser atraído por um objeto?
Desenvolvendo a aula: (35 min.)
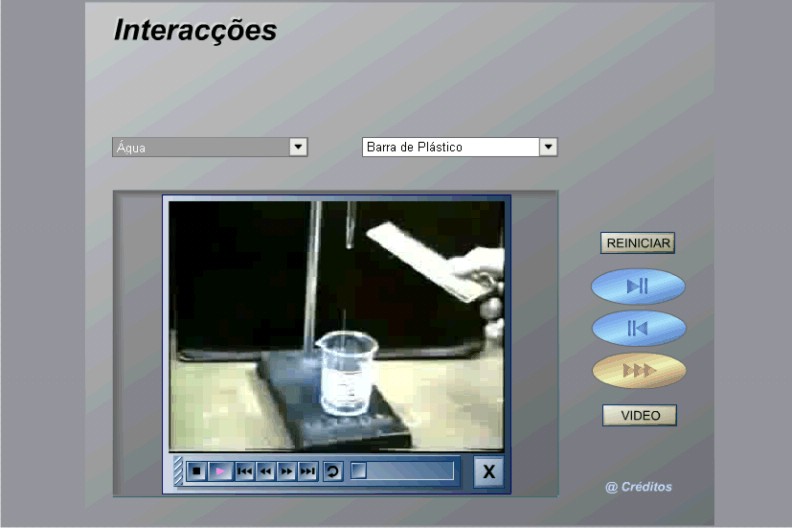
Após ouvir as respostas dos alunos, reproduza o vídeo sobre a polaridade da água (clique na seta e selecione: água). Pergunte aos alunos o que aconteceu? Pergunte também, por que a água foi atraída pelo objeto?
Explique aos alunos que, para ocorrer atração entre materiais, é necessária a existência de cargas de sinais opostos (+ ou -). Isso significa dizer que a água foi atraída por conter cargas opostas às do objeto.
Pergunte aos alunos: Por que algumas moléculas como as da água e da acetona são polares e outras como o ciclohexano são apolares?
Para responder a essa pergunta, explique aos alunos que os átomos dos elementos químicos apresentam diferentes intensidades de atração sobre os pares de elétrons em ligações covalentes. A eletronegatividade é uma grandeza que mede essa diferença de intensidade, a qual é responsável por diversas propriedades físicas e químicas das substâncias. A determinação dessa intensidade foi feita atribuindo valores relativos, que representam a diferença comparativa entre as intensidades dos átomos participantes de uma ligação covalente ao atrair elétrons ligantes. Sendo que o Flúor (F) é o elemento com a maior eletronegatividade (3,98 – 4,0) e o Frâncio é o elemento com menor eletronegatividade (0,7).
Após a explicação, peça para que os alunos abram o link da tabela periódica e, solicitando informações a eles, preencham informações da eletronegatividade de vários elementos, como exemplo, preencha a tabela a seguir:
| Elemento | Eletronegatividade |
| O | 3,5 |
| Cl | 3,0 |
Havendo uma diferença de eletronegatividade entre átomos ligantes, haverá uma distribuição de cargas entre os mesmos a qual pode ser medida pelo momento de dipolo elétrico (unidade debye). O sentido e a direção da distribuição da carga na ligação são indicados pelo vetor de momento de dipolo representado por  . Em moléculas com mais de uma ligação covalente os vetores de dipolo se somam, resultando em uma distribuição de cargas que corresponderá a um dipolo elétrico final. As moléculas cuja resultante dos dipolos de cada ligação for nula serão apolares e as demais serão polares.
. Em moléculas com mais de uma ligação covalente os vetores de dipolo se somam, resultando em uma distribuição de cargas que corresponderá a um dipolo elétrico final. As moléculas cuja resultante dos dipolos de cada ligação for nula serão apolares e as demais serão polares.
Para determinar essa resultante, deve-se fazer a soma vetorial dos dipolos de ligações, como ilustrado na figura a seguir para a molécula da água.
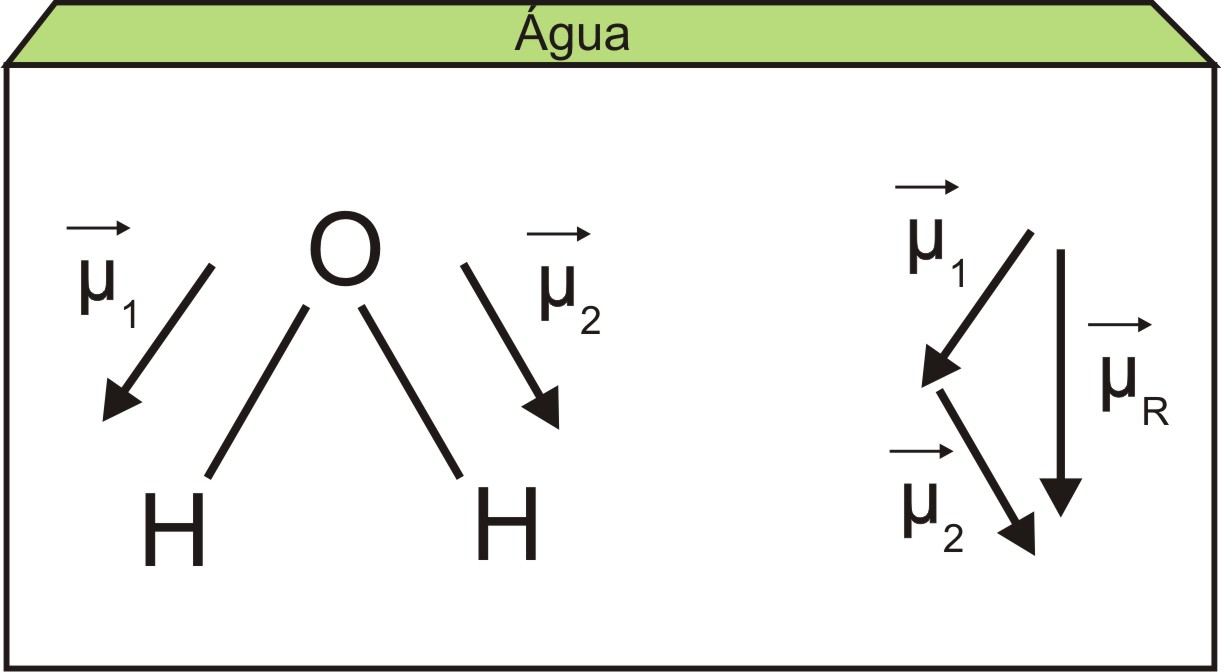
O vetor de momento dipolo é direcionado do átomo mais eletronegativo para o átomo menos eletronegativo. Após traçar todos os vetores de momento dipolo da molécula é necessário determinar a resultante desses vetores, onde: se esse vetor é igual a zero a molécula é apolar e se for diferente de zero a molécula é polar. Diante disso, temos que as moléculas que são polares serão atraídas pelo objeto eletrizado. Forneça exemplos mais exemplos para os alunos.
Após a explicação, peça para que os alunos executem a animação, porém alterando as substâncias e em seguida visualizando os vídeos.
Sistematização da aula (10min)
Peça aos alunos para elaborarem um relatório da exploração em que deverá conter as seguintes informações:
- Como determinar a polaridade de uma molécula;
- Como a eletronegatividade interfere na determinação da polaridade;
- Polaridade da molécula da água, da acetona, do ciclo hexano e do tetracloreto de carbono;
- Por que algumas substâncias foram atraídas pelo objeto eletrizado e outras não?
Avaliação
Sem estrelas 0 classificações
- Cinco estrelas 0/0 - 0%
- Quatro estrelas 0/0 - 0%
- Três estrelas 0/0 - 0%
- Duas estrelas 0/0 - 0%
- Uma estrela 0/0 - 0%
Denuncie opiniões ou materiais indevidos!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


