29/08/2008
Wildson Luiz Pereira dos Santos
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
O que o aluno poderá aprender com esta aula
• Identificar a natureza elétrica das interações dipolo-dipolo;
• Diferenciar interações intermoleculares: dipolo-dipolo, dipolo induzido e ligações de hidrogênio.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Estratégias e recursos da aula
Conteúdos específicos:
• Interações dipolo-dipolo;
• Interações dipolo-dipolo induzido;
• Ligações de hidrogênio.
Recursos educacionais:
• Site que apresenta simulações e vídeos sobre a polaridade da água e de outras substâncias clique no link para visualizar: nautilus.fis.uc.pt/cec/molecularium/pt/ligintermol/interaccoes/index.html;
• Site que apresenta simulação da interação das moléculas apolares. Clique no link para visualizar: nautilus.fis.uc.pt/cec/molecularium/pt/ligintermol/dipolo/index.html;

• Site que apresenta simulação da interação das moléculas polares. Clique no link para visualizar: chemmovies.unl.edu/ChemAnime/DIPOLED/DIPOLED.html;

Introduzindo a aula: (5 min.)
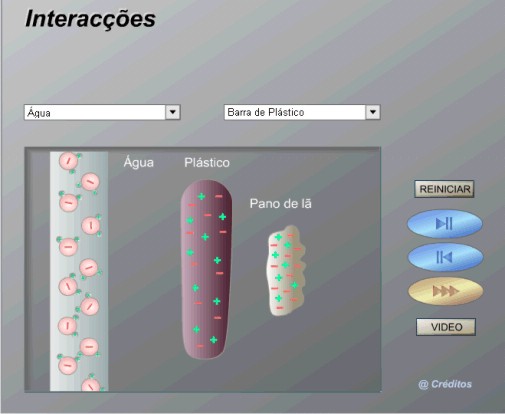
Inicie a aula a aula pedindo para que os alunos abram a simulação presente no site: http://nautilus.fis.uc.pt/cec/molecularium/pt/ligintermol/interaccoes/index.html. Pergunte aos alunos se algum líquido pode ser atraído por um objeto.
Desenvolvendo a aula: (25 min.)
Após ouvir as respostas dos alunos peça a eles que escolham a simulação da água e em seguida o vídeo. Pergunte-lhes o que aconteceu. Após as respostas dos mesmos, explique que a água foi atraída pela régua eletrizada. Isso ocorreu porque a água e a régua possuem polaridades diferentes, por isso ocorre a atração.
Peça para que os alunos escolham a acetona e executem a animação e o vídeo. Pergunte o que aconteceu. Pergunte tamb&eac ute;m se existe semelhança entre a molécula da acetona e a molécula de água. Após ouvir as respostas dos alunos, explique que as duas moléculas apresentadas são moléculas polares e, por isso, elas são atraídas pela régua.
Solicite aos alunos que executem a simulação e o vídeo das duas substâncias restantes, o ciclo-hexano e o tetracloreto de carbono. Pergunte a eles o que aconteceu. Pergunte também, se existe alguma semelhança entre essas duas moléculas e as moléculas da água e da acetona. Após as indagações dos alunos, explique que as moléculas do tetracloreto de carbono e do ciclo-hexano são moléculas polares, por isso a atração pela régua foi pequena.
Diga aos alunos que, para entender melhor a atração das moléculas de uma substância, é necessário estudar as forças intermoleculares. Essas interações são chamadas de interações de Van der Waals, em homenagem ao cientista holandês Johannes D. Van der Waals, autor da formulação matemática que permitiu o desenvolvimento desse estudo.
Peça para os alunos abrirem a simulação presente no site a seguir:
http://nautilus.fis.uc.pt/cec/molecularium/pt/ligintermol/dipolo/index.html. Peça-lhes que leiam as informações apresentadas. Pergunte a eles se as moléculas apresentadas pela simulação são polares ou apolares. Pergunte também, qual o nome das interações que ocorreram com as moléculas. Após ouvir as respostas dos alunos, explique que moléculas apolares como a do tetracloreto (CCl4), ao se aproximarem, induzem a formação de dipolos instantâneos. Como resultado, esses dipolos permitem uma maior interação entre as moléculas. Essa interação é chamada de dipolo-dipolo induzido. Essas interações são fracas e ocorrem em moléculas apolares.
Após as explicações, peça para os alunos abrirem a simulação presente no site: http://chemmovies.unl.edu/ChemAnime/DIPOLED/DIPOLED.html. A simulação está em inglês, por isso é necessário que o professor acompanhe a simulação. Pergunte aos alunos se a molécula apresentada pela simulação é polar ou apolar. Após ouvir-lhes as respostas, explique que as moléculas polares, devido à distribuição de suas cargas elétricas, possuem dipolos elétricos permanentes. Essa distribuição de cargas faz com que as moléculas interajam umas com as outras por atração eletrostática entre dipolos opostas, é o que acontece com a molécula de água (H2O). Essa interação molecular recebe o nome de dipolo-dipolo.
Explique aos alunos que existem tipos específicos das interações dipolo-dipolo, que são as ligações de hidrogênio. Esse tipo de interaçã o intermolecular ocorre em sub stâncias que possuem &aa cute;tomos de hidrogênio ligados a átomos de flúor, oxigênio ou nitrogênio. Nesses casos, graças às grandes diferenças de eletronegatividade, as ligações são muito p olarizadas. Como conseqüência, átomos de hidrogênio ficam com carga parcial positiva e são atraídos por átomos de flúor, oxigênio ou nitrogênio (possuidores de cargas de elétrons não ligantes) de moléculas vizinhas. Essas interações são muito fortes e mantém as moléculas mais unidas.
Para finalizar a aula, peça aos alunos que respondam as questões propostas na parte de sistematização da aula.
Sistematizando a aula: (20 min.)
Para sistematizar e consolidar os conteúdos explorados na simulação e nas explicações do professor, os alunos deverão responder às seguintes questões:
Questões da Animação
- Explique por que as moléculas da água são atraídas pela régua?
- Explique por que as moléculas do tetracloreto de carbono não são atraídas pela régua?
- Explique como ocorrem as ligações de hidrogênio. Dê exemplos.
- Diferencie as interações dipolo-dipolo induzido das interações dipolo-dipolo.
Sugestões de alternativas para o desenvolvimento da aula
Caso o professor não tenha à sua disposição um laboratório computacional e possua apenas um computador com um datashow, poderá mostrar a simulação para a turma.
Avaliação
Sem estrelas 0 classificações
- Cinco estrelas 0/0 - 0%
- Quatro estrelas 0/0 - 0%
- Três estrelas 0/0 - 0%
- Duas estrelas 0/0 - 0%
- Uma estrela 0/0 - 0%
Denuncie opiniões ou materiais indevidos!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


