28/08/2008
Ana Cristina de Almeida Sonza
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
O que o aluno poderá aprender com esta aula
• Relacionar as principais propriedades do vidro.
• Aplicar regra do octeto para prever a formação de íons.
• Conceituar íons.
• Conceituar ligação iônica.
• Fazer previsões de fórmulas químicas de compostos iônicos simples.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
• Modelo atômico de Rutheford.
Estratégias e recursos da aula
Conteúdos específicos:
- Óxidos iônicos e moleculares.
- Propriedades dos óxidos.
- Reciclagem de vidro.
Recurso educacional:
- Vídeo “De onde vem o vidro” do Ministério da Educação (duração: 04min 35s).
- Simulação sobre como é feito o vidro: http://www.labvirtq.fe.usp.br/simulacoes/quimica/sim_qui_vidracaria.htm
Preparando a aula:
Em aula anterior solicite os alunos que tragam utensílios de vidro de diferentes cores.
Introduzindo a aula: (5 a 10 min.) Colocar o vídeo do caco para motivação.
Esta aula poderá ser desenvolvida no laboratório de informática da escola, na própria sala de aula, ou sala ambiente, caso elas disponham de data show.
Inicialmente, peça aos alunos que separem os utensílios de vidro (trazidos de casa) e se organizem formando grupos com três componentes. Proponha questões que estimulem os alunos a explicarem o porquê do vidro se apresentar em diversas formas e cores. A partir das discussões dos alunos, introduza a aula dizendo a eles que irão assistir a um vídeo para que possam analisar o princípio da formação do vidro e, em seguida uma simulação no computador para relacionarem as ligações químicas nas suas substâncias constituintes.
Oriente os alunos para permanecerem em grupos, enquanto assistem ao vídeo:
Desenvolvendo a aula: (20 a 25 min.)
Após o vídeo o professor deve explicar aos alunos que as propriedades do vidro estão relacionadas com as interações entre os átomos, por isso, é importante estudar os diferentes tipos de interações. Diga aos alunos que na aula de hoje vamos estudar um tipo de interação que está presente entre os átomos de algumas substâncias usadas na produção do vidro. Em seguida peça para os alunos iniciarem a simulação pre sente no site: http://www.labvirtq.fe.usp.br/simulacoes/quimica/sim_qui_vidracaria.htm.
Após a conclusão da simulação, pergunte aos alunos quais são os principais componentes do vidro? Após ouvir as respostas dos alunos, explique que o vidro é formado por uma substância base, a sílica (SiO2), e são adicionados a ela alguns compostos iônicos como óxido de cálcio (CaO) e óxido de chumbo (PbO). Em seguida, pergunte aos alunos o que são compostos iônicos? Após ouvir as respostas dos alunos, explique que os compostos iônicos são formados devido a um dos seus átomos atrair mais os elétrons do que o outro, ou seja, possuir maior eletronegatividade. No composto iônico Cloreto de sódio, sal de cozinha, que possui fórmula molecular NaCl, temos que: quando os dois átomos se aproximam o elétron do último nível do sódio é atraído mais fortemente pelo núcleo do átomo de cloro, que tem a maior tendência de atrair elétrons (eletronegatividade). Como conseqüência o elétron é transferido do átomo de sódio para o de cloro. Nesse processo, o átomo de sódio fica com um elétron a menos e o de cloro com um a mais, formando assim os íons, como ilustrado na figura abaixo:
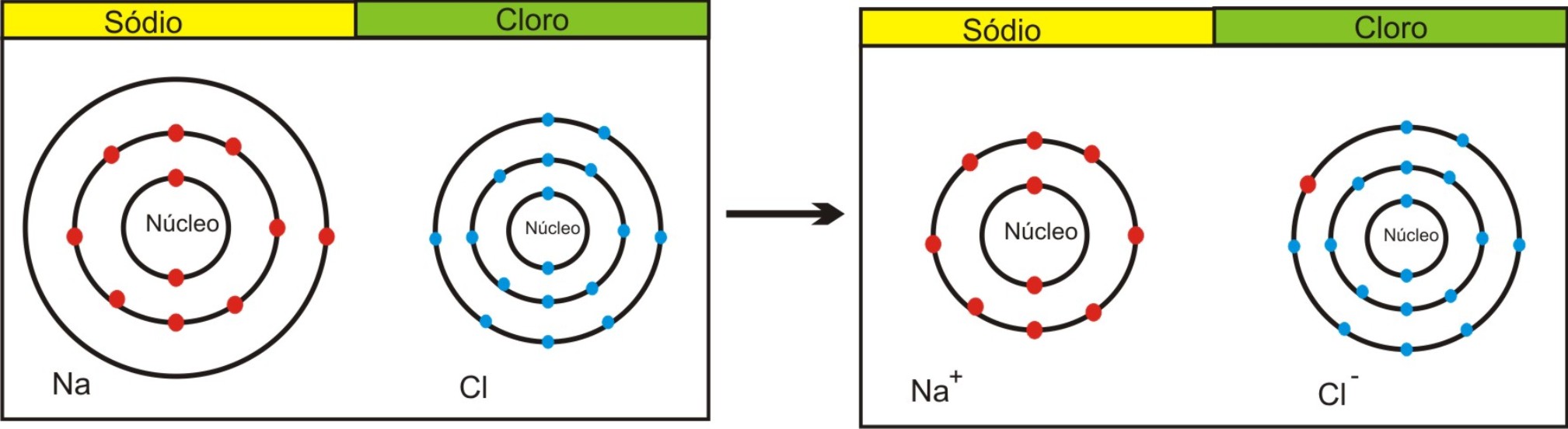
Com a formação dos íons, passa a existir atração eletrostática entre essas espécies químicas: os íons positivos (cátions) atraem os negativos (ânions). Essa interação entre os cátions e ânions é denominada ligação iônica.
Para finalizar a aula peça para os alunos responderem as questões presentes na parte de sistematização da aula.
Sistematizando a aula: (20 min.)
Após a simulação, peça aos alunos que respondam as questões sugeridas abaixo para que eles possam relacionar:
- O processo de formação do vidro com os óxidos que o compõe.
- A moldagem e coloração do vidro com as suas propriedades.
O professor deverá circular na sala verificando se os grupos estão compreendendo as questões solicitada s.
Para responder as perguntas, caso necessário os alunos poderão refazer a simulação no computador ou rever o vídeo.
- Identificar os principais componentes que formam o vidro.
- Relacionar as principais propriedades do vidro.
- Como ocorre a formação natural do vidro?
- Quais são as principais substâncias que formam o vidro?
- Quais as propriedades do vidro?
- Por que o vidro pode ser moldado em diferentes formas?
- Quais as diferenças entre o vidro comum (incolor) e os vidros coloridos?
- Por que o vidro é utilizado para o armazenamento de alimentos?
- Qual é a importância da reciclagem do vidro para o meio ambiente?
- Como se formam os vidros temperados?
- Como são formados os compostos iônicos?
- Faça o desenho representando a formação da ligação iônica da molécula PbO. Identifique os íons formados.
Recursos Educacionais
| Nome | Tipo |
|---|---|
| De onde vem o vidro? | Vídeo |
Avaliação
Cinco estrelas 2 classificações
- Cinco estrelas 2/2 - 100%
- Quatro estrelas 0/2 - 0%
- Três estrelas 0/2 - 0%
- Duas estrelas 0/2 - 0%
- Uma estrela 0/2 - 0%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
Marcos Aurélio Veras da Fonseca, GUILHERME GOUVEIA CEJA , Ceará - disse:
mavfonseca65@hotmail.com24/03/2010
Cinco estrelasOtima aula, muito bem elaborada. Parabéns.
-
cristiane alves, Escola Andre avelino ribeiro.. , Mato Grosso - disse:
cristiane.alves@seduc.mt.gov.br24/03/2010
Cinco estrelasA aula foi muito bem estruturada de maneira que os alunos entenderão o conteúdo principal a partir dos videos e compreenderão sem dúvidas o objetivo da aula.. Ao mostrar os modelos, se possivel que sejam animados também isso facilitará a compreensão dos alunos ao tentarem visualizar os eletrons nas orbitas dos átomos..
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


 De onde vem o vidro?
De onde vem o vidro?