18/12/2008
Ezequiel Menta
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Biologia | Origem e evolução da vida |
| Ensino Fundamental Final | Ciências Naturais | Vida e ambiente |
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
O que o aluno poderá aprender com esta aula
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Estratégias e recursos da aula

Nesta aula o professor poderá iniciar falando que as substâncias presentes em nosso planeta são encontradas como misturas (soluções) que vão desde as microscópicas células vivas até os gigantescos mares e oceanos, além disso, necessárias ao preparo dos alimentos. Neste contexto, está a água e nela podemos encontrar dispersas muitas substâncias (açúcar, medicamentos, substâncias tóxicas, sal, germens, etc.) de grande importância para a vida animal e vegetal. Encontramos também diferentes compostos no sangue e na urina.
Interdisciplinaridade
O professor de ciências ou biologia pode tratar dos componentes químicos presentes nas soluções de urina e de sangue.
Solicite aos estudantes que tragam livros para a sala de aula para que pesquisem outros conceitos de dispersões. Após pesquisarem, ofereça aos estudantes a tabela "Dispersões: principais características" para que comparem com as informações coletadas na pesquisa.
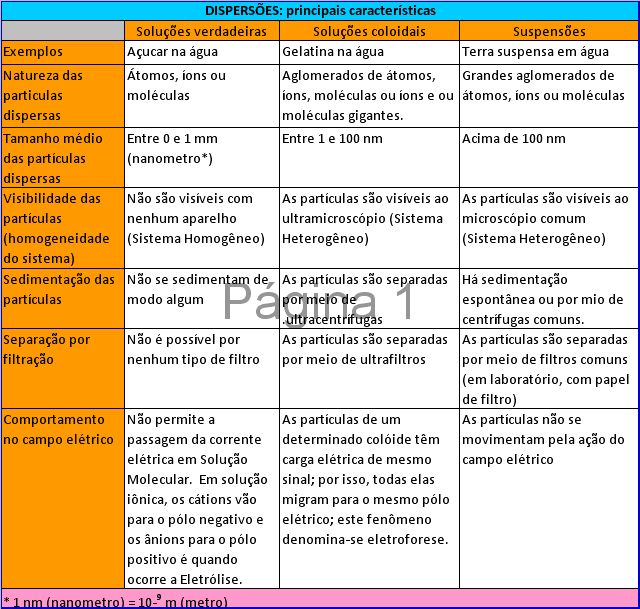
Antes que iniciem a atividade, explique que para Feltre, (1997) as dispersões são sistemas nos quais uma substância está disseminada, sob forma de pequenas partículas, numa segunda substância.
Em seguida pergunte: o que é solução? Veja que informações eles possuem, amplie as discussões a partir de outros questionamentos.
Após o debate você poderá explicar a definição de Soluções e a sua classificação.

Soluções: são misturas homogêneas de duas ou mais substâncias e se distribuem em três tipos: (sólido + líquido); (gás + líquido); (gás + gás). Apresente alguns exemplos de soluções, o café com leite, a água do mar, o xarope medicinal (solução de sacarose saturada), urina (solução de diversos sais e toxinas) refrigerante artificial, as tintas (à base de água e a óleo). Informe que as partículas dispersas do soluto são íons ou íons e moléculas. Os íons são os responsáveis pela condução da corrente elétrica numa solução, que as soluções iônicas ou eletrolíticas conduzem a corrente elétrica e que são exemplos: a água e sal (cloreto de sódio) e água e ácido clórico. É importante falar também que a solução molecular também chamada de solução não-eletrolítica não conduz corrente elétrica. Exemplo: água e açúcar.

Após as explicações, encaminhe os estudantes para o laboratório de informática para que acessem a animação “Quem apagou a luz?”. Por meio desta animação os estudantes poderão compreender o conceito de soluções iônica e molecular, através da preparação de soluções que conduzem ou não corrente elétrica.

2ª Aula

Solicite aos estudantes para que se organizem em equipes, façam alguns testes em diferentes tipos de soluções a fim de verificar se estas conduzem ou não corrente elétrica quando dissolvidas em água. Ao final do experimento as equipes deverão produzir um relatório.

Oriente os estudantes para que leiam o texto abaixo e respondam a pergunta.
Como já vimos, encontramos na natureza diferentes tipos de compostos químicos constituídos por átomos ou íons de dois ou mais elementos que se combinam. Dentre eles destacamos: a água (H2O), o sal dissolvido na água do mar (MgCl2), constituinte da areia e das rochas (SiO2), o minério de alumínio, bauxita (Al2O3), minério de ferro, hematita (Fe2O3) e constituinte dos nossos ossos Ca3(PO4)2. Outros elementos são encontrados na forma livre como constituintes do ar atmosférico: Ar e Ne (que são gases nobres); o nitrogênio (N2), oxigênio (O)2. O ouro (Au), é encontrado na natureza como metal. Pergunta: Quais são as principais características e propriedades que você conhece dos compostos iônicos, covalentes e dos metais?
Solicite que publiquem os resultados em um Blog. Para tanto poderão acessar o endereço: <https://www.blogger.com/start>
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Quem apagou a luz? | Animação/simulação |
Recursos Complementares
Avaliação
Sem estrelas 0 classificações
- Cinco estrelas 0/0 - 0%
- Quatro estrelas 0/0 - 0%
- Três estrelas 0/0 - 0%
- Duas estrelas 0/0 - 0%
- Uma estrela 0/0 - 0%
Denuncie opiniões ou materiais indevidos!
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


 Quem apagou a luz?
Quem apagou a luz?