28/11/2013
Alfredo Luis Martins Lameirão Mateus
| Modalidad / Nivel de Enseñanza | Disciplina | Tema |
|---|---|---|
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
| Ensino Médio | Química | Transformações: caracterização, aspectos energéticos, aspectos dinâmicos |
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
O que o aluno poderá aprender com esta aula
O objetivo da aula é permitir ao aluno descobrir que existe uma ordem na tendência de uma substância ganhar ou perder elétrons. Por meio desta atividade, o aluno irá investigar qual halogênio é o melhor agente oxidante, será capaz de descrever os sistemas inicial e final após observar diversas misturas e perceber em quais casos houve uma transformação química. Além disso, ele irá escrever as equações químicas das reações que ocorrerem e interpretar os resultados de modo a perceber que existem diferentes potenciais de oxidação para os elementos, correlacionando o resultado com a sua posição na tabela periódica.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Conhecimento básico sobre reações químicas: o que são, quais as evidências de que uma reação está ocorrendo e como representar uma reação química.
Estratégias e recursos da aula
Esta é uma atividade pensada para uso no início do tópico de reações de oxirredução.
Consiste de preparos de várias misturas contendo os halogênios cloro, bromo e iodo com soluções dos seus respectivos ânions: cloreto, brometo e iodeto. Os alunos deverão observar essas soluções e tentar interpretar aquilo que é observado.
Materiais
- Água sanitária
- Ácido clorídrico
- Tintura de iodo
- Água de bromo (veja como preparar abaixo)
- Brometo de potássio ou brometo de sódio
- Cloreto de sódio (sal de cozinha)
- Iodeto de potássio
- Tubos de ensaio e suporte
- Conta-gotas
ATENÇÃO! Dois dos halogênios (cloro e bromo) são muito perigosos e difíceis de se manipular. Por isso, ao invés de usar os elementos na sua forma pura, iremos preparar pequenas quantidades dos elementos em solução.
ATENÇÃO! A água sanitária é corrosiva e alcalina. A solução de ácido clorídrico 1 mol/L pode irritar a pele. Lave bem as mãos após o uso e evite contato com a pele. Use apenas quantidades pequenas dos reagentes.
ATENÇÃO! O bromo é um elemento altamente tóxico. Evite o contato com a pele e não respire os vapores. Faça a reação com quantidades pequenas e em local ventilado. O uso de luvas e óculos de segurança é recomendado.
Inicialmente, prepare soluções dos sais (cloreto de sódio, brometo de potássio e iodeto de potássio) dissolvendo cerca de 1 g em 10 mL de água.
Obtendo o cloro
Em um tubo de ensaio, misture 2 mL de ácido clorídrico 1 mol/L e 2 mL de água sanitária comercial.
Obtendo a água de bromo
Em um tubo de ensaio, misture 4 mL da solução de cloro preparada na etapa anterior e 2 mL da solução de brometo de potássio.
Trabalhando com os halogênios
Brometo + cloro
Em um tubo de ensaio, coloque 1 ou 2 mL da solução de brometo (pode ser brometo de potássio ou de sódio). Acrescente 4 mL da solução de cloro, gota a gota, até observar a mudança de cor.
Iodeto + cloro
Em um tubo de ensaio, coloque 1 ou 2 mL da solução de iodeto de potássio. Prepare mais 4 mL da solução de cloro preparada anteriormente e adicione-os, gota a gota, ao tubo de ensaio, até observar a mudança de cor.
Cloreto + bromo
Em um tubo de ensaio, coloque 1 ou 2 mL da solução de cloreto de sódio. Adicione a água de bromo gota a gota e observe se houve alguma mudança.
Iodeto + bromo
Repita o procedimento acima, substituindo a solução de cloreto de sódio pela solução de iodeto de potássio.
Brometo + iodo
Em um tubo de ensaio, coloque 1 mL da solução de brometo de potássio. Acrescente a tintura de iodo gota a gota. Observe se houve alguma mudança.
Cloreto + iodo
Em um tubo de ensaio, coloque 1 mL da solução de cloreto de sódio. Acrescente a tintura de iodo gota a gota. Observe se houve alguma mudança.
Após realizarem os testes ou assistirem ao vídeo, os alunos devem anotar suas observações em um quadro semelhante ao representado a seguir.
Quadro 1: Resultados dos experimentos
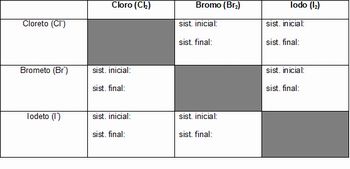
Depois de realizado o experimento, ou exibido o vídeo, sugerimos que o professor proponha as questões para discussão a seguir.
Questões para discussão
1. Escreva as equações químicas que representam o que ocorreu nos tubos em que uma mudança foi percebida.
Resposta:
Cl2 + 2 Br-  Br2 + 2 Cl-
Br2 + 2 Cl-
Cl2 + 2 I-  I2 + 2 Cl-
I2 + 2 Cl-
Br2 + 2 I-  I2 + 2 Br-
I2 + 2 Br-
2. Coloque os três elementos em ordem da sua capacidade de transformar os ânions em espécies neutras.
Resposta:
Cl2 > Br2 > I2
3. Consulte uma tabela periódica e localize os elementos com os quais estamos trabalhando. O que você acha que aconteceria se fizéssemos a reação do flúor (F2) com os ânions dos outros halogênios? Como poderíamos explicar o comportamento dos halogênios em relação à sua posição na tabela periódica?
Resposta:
A ordem de cima para baixo na família (grupo ou coluna) dos halogênios é flúor, cloro, bromo e iodo. Percebemos que o cloro consegue oxidar o brometo e o iodeto. O bromo só consegue oxidar o iodeto e o iodo não consegue oxidar nenhum dos outros. Assim, podemos concluir que quanto mais para cima na tabela, maior é a tendência em ganhar elétrons e ser o melhor oxidante.
O flúor está localizado acima do cloro na tabela periódica. Percebemos que o cloro consegue reagir com todos os ânions dos elementos abaixo dele na tabela. O flúor será capaz de reagir com o cloreto, com o brometo e com o iodeto e é o melhor oxidante de todos eles.
Isso ocorre pois quanto mais acima em uma coluna, mais próximos estarão os elétrons da última camada do núcleo, já que cada vez que descemos um período da tabela, acrescentamos uma camada no átomo. Assim, existe uma maior relação carga / raio, fazendo com que o pequeno flúor tenha grande tendência por pegar elétrons e o iodo tenha uma tendência muito menor.
4. Observe as semi-reações abaixo:
Cl2 + 2 e-  2 Cl-
2 Cl-
Br2 + 2 e-  2 Br-
2 Br-
I2 + 2 e-  2 I-
2 I-
O elemento que possui maior tendência para ganhar um elétron e se transformar no ânion é o melhor agente oxidante. O ânion que possui maior tendência para perder um elétron e se transformar no átomo neutro é o melhor agente redutor. Qual dos elementos acima é o melhor agente oxidante e qual é o melhor agente redutor?
Resposta:
O elemento cloro (Cl2) é o melhor oxidante.
O ânion iodeto (I-) é o melhor redutor.
Tabela de resultados dos experimentos – exemplo de preenchimento
|
|
Cloro |
Bromo |
Iodo |
| Cloreto
|
|
não ocorre reação |
não ocorre reação |
| Brometo
|
solução laranja |
|
não ocorre reação |
| Iodeto
|
solução marrom |
solução marrom |
|
Recursos Complementares
Você pode realizar o experimento com os alunos ou utilizar um vídeo que mostra o preparo das soluções. O vídeo do experimento está disponível no Banco Internacional de Objetos Educacionais (BIOE) e pode ser acessado no endereço a seguir.
Avaliação
Sugerimos que o professor avalie por meio do desempenho dos alunos e das respostas dadas por eles às questões propostas na atividade.
Sem estrelas 0 calificaciones
- Cinco estrelas 0/0 - 0%
- Quatro estrelas 0/0 - 0%
- Três estrelas 0/0 - 0%
- Duas estrelas 0/0 - 0%
- Uma estrela 0/0 - 0%
Denuncia opiniones o materiales indebidos!
- Sugerencias de clases
- Clases
- Colecciones de clases
- Crear clase
- Crear individual
- Crear em equipo
- Accede tus equipos
- Mis clases
- Orientaciones
- Creando equipos
- Pistas para producción de clases
- Reflexiones pedagógicas
- Utilizando la herramienta
- Artículo: portal educacional
- Estadísticas de uso del Portal
- Clases Estadísticas
- Estadísticas de recursos
- Estadísticas de visitas
- Recursos utilizados en las clases de
- Reflexiones pedagógicas
- Informaciones de cursos
- Cursos
- e-Proinfo
- Materiales de curso
- Materiales de estudio
- Artículos y Publicaciones
- Asuntos relevantes
- Opiniones
- Ciencias de la vida cotidiana
- Destaca Internacional
- Consejos prácticos
- La educación profesional y tecnológica
- Entrevistas
- Estrategias pedagógicas
- Las innovaciones tecnológicas
- Los materiales del curso
- Acontecimiento Materiales
- Directrices y directivas
- Parámetros y referencias
- Programas en los vídeos
- Tutoriales
- TVescola
- Cuadernos didáticos
- Colecciones de recursos
- Recursos educacionales
- Sitios temáticos
- Tv escuela en vivo
- Herramienta del portal
- Foro
- Portal em Youtube
- Compartiendo presentaciones
- Herramientas por internet
- Blog
- Compartir videos
- La comunicación en línea
- Crear y compartir presentaciones
- Editar y compartir fotos
- Escritura colaborativa
- Únete a una comunicade
- Hilo
- Organizar y compartir tus favoritos
- Podcast
- Radio / TV y otra universidad
- Redes Sociales
- Robot Ed
PLATAFORMA FREIRE
- Bibliotecas
- Proinfo integrado de capacidad
- cultura
- Diccionarios, traductores y enciclopedias
- La educación inclusiva
- Geoprocessamentos
- La inclusión digital
- Infografía
- Juegos educativos
- Periódicos
- Museos
- Observatorios y planetarios
- Organizaciones gubernamentales
- Las plataformas educativas
- Portales educativos y otros
- MEC Portal
- Profesores Premio de Brasil
- Producciones de los docentes
- Proyectos de Escuelas
- Proyectos innovadores
- Los proyectos sociales y educativos
- Escuela de Radio
- Recursos digitales
- Revistas
- Búsqueda Sitios
- Sitios portal temático y TVescola
- Software de edición y otros
- Software educativo
- Un ordenador por alumno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus


