25/11/2009

|

|

|
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Química | Modelos de constituição: substâncias, transformações químicas |
O que o aluno poderá aprender com esta aula
Após explorar os recursos e textos desta aula o estudante deverá ser capaz de compreender sobre reações endotérmicas e exotérmicas quando ocorrem e de que forma ocorrem.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
É necessário que o estudante saiba como ocorrem as reações químicas.
Estratégias e recursos da aula

Quando se aquece o carbonato de cálcio e este se decompõe em óxido de cálcio e dióxido de carbono que tipo de reação temos: endotérmica ou exotérmica?



Por meio do vídeo “Reação Exotérmica - Permanganato de Potássio e Glicerina“ é possível compreender como ocorre uma reação exotérmica.
http://www.youtube.com/watch?v=Gg0kC8_84Ug

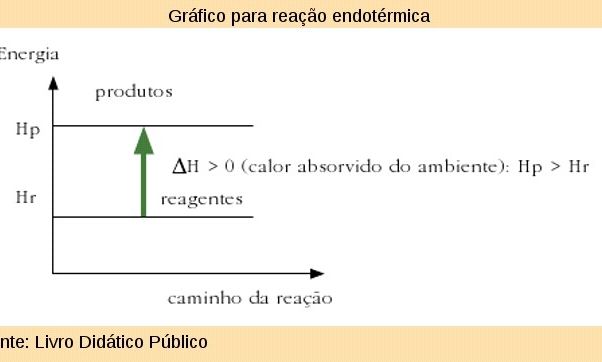
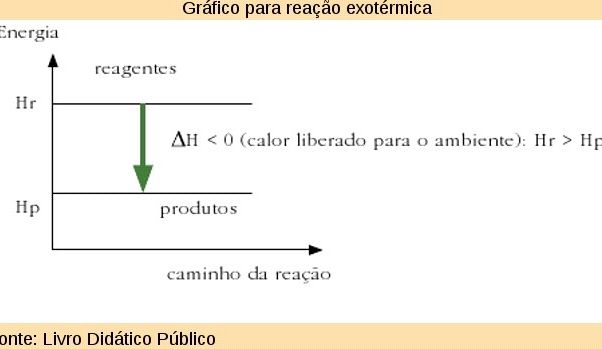
Reação exotérmica: reação química que libera calor, sendo, portanto, a energia final dos produtos menor que a energia inicial dos reagentes. Disso se conclui que a variação de energia é negativa.
Exemplo:
A água ao se transformar em gelo representa uma reação exotérmica tendo em vista a perca de calor.
http://www.diaadia.pr.gov.br/tvpendrive/arquivos/File/imagens/4quimica/7grafreaendo.jpg

O vídeo “Entrando numa fria“ apresenta uma experiência com a reação endotérmica.
http://www.youtube.com/watch?v=IZ5nlEI-p4o

Reação Endotérmica: reação química que absorve calor, utiliza energia do exterior. Transferida num sistema fechado sob a forma de calor, capta energia para suas vizinhanças. Por se tratar de um sistema isolado, a temperatura diminui durante a reação até que alcance o equilíbrio. É portanto, a energia final dos produtos maior que a energia inicial dos reagentes. A variação de energia é positiva.
Exemplo:
Quando se ferve um copo d´agua se tem uma reação endotérmica, pois a água absorve o calor ao atingir o ponto de ebulição e se transformar em vapor.
Representação química da obtenção da cal viva.
CaCO3 ----> CaO + CO2
http://www.diaadia.pr.gov.br/tvpendrive/arquivos/File/imagens/4quimica/7grafreacaoexo.jpg
Exercício1:(UFMG ) Um palito de fósforo não se acende, espontaneamente, enquanto está guardado. Porém basta um ligeiro atrito com uma superfície áspera para que ele, mediatament e, entre em combustão, com emissão de luz e calor.Considerando-se essas observações, é CORRETO afirmar que a reação:
A) é endotérmica e tem energia de ativação maior que a energia fornecida pelo atrito.
B) é endotérmica e tem energia de ativação menor que a energia fornecida pelo atrito.
C) é exotérmica e tem energia de ativação maior que a energia fornecida pelo atrito.
D) é exotérmica e tem energia de ativaç ão menor que a energ ia fornecida pelo at rito.
Exercício2:
A reação é exotérmica ou endotérmica?
Ao preparar uma solução de hidroxido de sodio, um estudante dissolveu 1,0 mol dessa base em água, completou o volume para 1,0 litro e notou que o recipiente usado para a dissolução ficou muito quente. Essa é uma reação exotémirca ou endotérmica?

No laboratório de química, solicite aos estudantes que desenvolvam o experimento abaixo. No momento em que desenvolvem a ação devem produzir um relatório que deverá se tornar disponível em um blog.
Após promova um debate e incentive-os a apontarem outros exemplos.
http://educar.sc.usp.br/quimapoio/fotoexoII.html
Recursos Complementares
http://www.fisica.net/quimica/resumo19.htm
http://www.conecteeducacao.com/escconect/medio/QUI/QUI04020200.asp
No endereço abaixo é possível pesquisar sobre o tema.
http://www.ufsm.br/nitrico/site/alunos/resumo_termoquimica.pdf
http://www.quimica.net/emiliano/vestibucast/termoquimica.pdf
O site abaixo trata das transformações exotérmicas e endotérmicas.
Avaliação
A avaliação poderá ser feita pela participação dos alunos em todos os passos da confecção dos gráficos que representem as reações endotermicas e exotérmicas. Uma forma interessante de avaliar é por meio da rubrica. Rubricas representam uma forma de avaliação autêntica, pois vai além da simples mensuração de notas. O professor estabelece critérios que cada trabalho deverá ter, e conforme os alunos cumpram estes critérios (totalmente, em parte, ou de maneira insuficiente) atribui-se um nível com um valor correspondente. Por fim, entendemos que a avaliação deve ser feita a partir das produções dos estudantes e apresentação das atividades sugeridas na aula ainda outras que o profissional julgar conveniente e que os sujeitos da aprendizagem devam ser comunicados com antecedência sobre o processo no qual estão inseridos.
Cinco estrelas 1 classificações
- Cinco estrelas 1/1 - 100%
- Quatro estrelas 0/1 - 0%
- Três estrelas 0/1 - 0%
- Duas estrelas 0/1 - 0%
- Uma estrela 0/1 - 0%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
frank, unics , Paraná - disse:
franklin_willian@hotmail.com01/01/2011
Cinco estrelasOtimo, pois dá condiçoes do aluno distinguir as reaçoes em discução
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus

