02/06/2010
Suelen Fernanda Machado
| Modalidade / Nível de Ensino | Componente Curricular | Tema |
|---|---|---|
| Ensino Médio | Língua Portuguesa | Gêneros discursivos e textuais: narrativo, argumentativo, descritivo, injuntivo, dialogal |
| Ensino Fundamental Final | Ciências Naturais | Vida e ambiente |
| Ensino Fundamental Final | Ciências Naturais | Tecnologia e sociedade |
| Educação Profissional | Controle e Processos Industriais | Técnico em Análises Químicas |
| Ensino Médio | Química | Propriedades das substâncias e dos materiais |
| Educação Profissional | Controle e Processos Industriais | Técnico em Química |
O que o aluno poderá aprender com esta aula
Deverão aprender como se representa a estrutura molecular dos ácidos carboxílicos e dos esteres, o conceito de reação de saponificação; definir e relacionar as principais propriedades dos sabões; preparar sabão simples.
Duração das atividades
Conhecimentos prévios trabalhados pelo professor com o aluno
Os alunos deverão saber sobre funções inorgânicas: bases; funções orgânicas: álcool e éster; grupos funcionais orgânicos – hidrocarbonetos; ligações covalentes; reação química e representação das substâncias polares e apolares.
Na aula anterior solicite aos alunos que pesquisem em casa os contéudos acima e registrem no caderno pois, serão questionados ao longo desta aula.
Estratégias e recursos da aula
Professor, leve os alunos para o laboratório de informática e organize-os em grupos de 3 pessoas. Solicite que acessem o link abaixo, respondam as questões e anotem as respostas para que confiram a partir da explicação do conteúdo. Pergunte às equipes que alternativas escolheram para cada questão desta maneira, você verifica os conhecimentos prévio dos alunos sobre sabão e sabonete. Link: http://www.dolceta.eu/portugal/Mod5/spip.php?article420
Após responderem, explique que o sabão é um sal de ácido carboxílico, que por possuir uma longa cadeia carbônica em sua estrutura molecular, é capaz de se solubilizar tanto em meios polares quanto em meios apolares. É um tensoativo, ou seja, reduz a tensão superficial da água fazendo com que ela "molhe melhor" as superfícies.
Fonte: http://pt.wikipedia.org/wiki/Saponifica%C3%A7%C3%A3o
Organize os alunos em equipes de no máximo 3 alunos. Conte a eles a situação-problema “As donas de casa normalmente associam a eficiência de um sabão com a quantidade de espuma que a mesma provoca” e questione: esta idéia é correta ou incorreta? Por quê? Inicie uma “roda da conversa”. Após dialogarem, explique que por si só o sabão não limpa. Essa aparente contradição pode ser entendida porque no sabão está presente o agente umectante que diminue a tensão superficial observada nos solventes, permite maior contato dos corpos com os líquidos, é o que realmente limpa.
Na sala de aula, organize os alunos em duplas. Explique que na fabricação de detergente são utilizadas substâncias derivadas do petróleo. No processo de fabricação de sabões se usa como matéria prima óleos ou gordura animal cujo base e a reação de saponificação. Saponificação é qualquer reação de um éster com uma base para produzir um álcool e o sal de ácido. Exemplifique no quadro como ocorre esta reação.
| éster + base saponificação sabão + álcool O O II II R - C - O - R + NaOH <=> R - C - O - Na + R - OH |
| Ácido graxo Hidróxido de sódio (sal de ácido graxo) Glicerol Sabão |
Neste momento, trabalhe os ácidos carboxílicos e o grupo funcional ester.
Ácidos carboxílicos: fale para os alunos que a pele libera ácidos carboxílicos cuja mistura dá o cheiro característico de cada um, podendo ser percebido especialmente pelos cães utilizados pela polícia para realizar investigações. São ácidos orgânicos caracterizados pela presença do grupo funcional carboxila. São tipicamente representados como COOH. Classificam-se em monoácidos ou poliácidos, dependendo do número de radicais carboxila presentes na molécula.
Explique que os ésteres são derivados de ácidos pela substituição do hidrogênio do ácido por um radical orgânico. São substâncias comuns na natureza, encontradas nos óleos e nas gorduras, nas essências de frutas, de madeiras e de flores; nas ceras como a de carnaúba e a de abelhas; nos fosfatídeos como os existentes no ovo e no cérebro. É representada por uma cadeia carbônica contendo de 12 a 18 átomos de carbono. Podem ser obtidos quando for o caso, pela reação entre ácido carboxílico e álcool.
Link: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=11877
Explique também que os ésteres mais importantes são os de ácidos carboxílicos.
a) CH3COO - CH3 → Acetato de metila ou etanoato de metila
b) CH3 - CH2 - COO - CH2 - CH3 → propanoato de etila
c) CH3 - COO - CH2 - CH2 - CH2 - CH3 → Etanoato de butila
d) CH2 = C (CH3) - COO - CH3 → metil propenoato de metila, o monômero do acrílico (plástico).
Como age o sabão?
A molécula de sabão possui uma característica especial: tem uma ponta polar (cabeça) que apresenta carga e uma ponta apolar (cauda) que não tem carga (ver figura abaixo). Na gota de óleo é formado uma porção de átomos de carbono ligados. Quando se coloca sabão na água, como a molécula da água também tem cargas, ela atrai a parte da “cabeça”. A parte da cauda ficará livre. Essas caudas irão se atrair entre si, formando bolinhas minúsculas, chamadas micelas.Quando o sabão está em atrito com algo, a sujeira é quebrada em pedacinhos, que ficam dentro das micelas. Desta forma não se pode lavar o óleo ou a gordura só com água porque na água líquida as moléculas de água estão ligadas umas às outras
Disponível em: http://www.cienciamao.if.usp.br/dados/t2k/_quimica_qui43.arquivo.pdf. Acesso em: 24.mai.2010.
Organize os alunos no laboratório de informática de modo que ocupem todos os computadores e solicite aos alunos acessem os recursos indicados, leiam o roteiro e desenvolvam as atividades.
Roupa suja se lava em casa - Link: http://portaldoprofessor.mec.gov.br/fichaTecnica.html?id=17157
Roupa suja se lava na Escola Link: http://objetoseducacionais2.mec.gov.br/handle/mec/5174
Roteiro
a) Se o sabão é feito de óleos e gorduras, como é capaz de limpar superfícies engorduradas?
b) Se óleos são insolúveis em água, como é possível retirá-los usando água e sabão?
c) Como o sabão age no processo de eliminação da "sujeira" (gordura)?
d) Qual a finalidade de se adicionar ácido durante a preparação do sabão?
e) Qual a diferença entre óleos e gorduras?
f) Por que se utiliza da base forte, como a soda cáustica para produzir sabão?
g) Qual é o subproduto da reação de saponificação e qual é a sua aplicação?
h) Indique a função orgânica existente no sabão.
i) O que são os radicais nas moléculas orgânicas?
j) Qual propriedade dos sabões faz com que eles removam a gordura?
Obs.: as respostas deverão ser entregues para o professor para compor a avaliação.
Link: http://objetoseducacionais2.mec.gov.br/handle/mec/5893
Relatório
Professor, sugerimos que os estudantes, se organizem em equipes de no máximo 5 pessoas e elaborem o relatório utilizando o editor de textos colaborativos disponível no Google Docs. Para auxiliar na utilização da ferramenta, há um tutorial no
link: http://docs.google.com/Doc?docid=dcdf798z_12chsmbcdf&hl=pt_BR
Roteiro para observação:
a) o que ocorreu ao adicionar 5 gotas de óleo mineral com água, e agitar?
b) que tipo de mistura se formou entre o óleo e a água?
c) o que ocorre ao adicionar um pequeno pedaço do sabão obtido na primeira etapa, quando medimos o pH aproximado da amostra com papel indicador?
Classifique como verdadeira (V) ou falsa (F) cada uma das afirmações a seguir:
a) ( ) A força entre moléculas de óleo é igual à força entre moléculas de água.
b) ( ) Detergentes não causam poluição.
c) ( ) Detergentes podem misturar-se com água e óleo.
d) ( ) As moléculas de detergente têm uma cadeia de átomos de carbono.
e) ( ) Detergentes são formados de moléculas que têm uma parte que atrai moléculas de água e outra que atrai moléculas de óleo.
Assinale com um X a correta:
As gorduras são constituídas essencialmente de: a) éteres b) aldeídos c) ésteres d) aminoácidos e)cetonas
(Fuvest-SP) Analise as 3 reações e assinale uma das cinco alternativas indicadas.
1) de ácidos graxos com hidróxido de sódio; 2) de álcool com ácido sulfúrico concentrado;
3) de celulose com ácido clorídrico.
a) açúcar, éter, sabão. b) açúcar, sabão, éter. c) éter, açúcar, sabão. d) sabão, éter, açúcar. e) sabão, açúcar, éter.
Esta atividade pode ser desenvolvida como avaliação. Proponha aos alunos que pesquisem sobre o conceito, propriedades, fórmulas, aplicação no dia a dia ácidos graxo; bases; éster; esterificação; etanol; gordura; lípideos (óleos e gorduras), façam anotações e postem em uma PBKWork´s. Este recurso é uma ferramenta eletrônica que permite construir páginas web, permite que múltiplos usuários façam edições e alterem seu conteúdo com facilidade por usuários leigos. Pode ser acessada no link: http://pbworks.com/ Para trabalhar com a PBKWork´s há um vídeo tutorial disponível em http://www.youtube.com/watch?v=gy_MM97R5QI
Site para pesquisa: http://www.fcfar.unesp.br/alimentos/bioquimica/praticas_lipidios/saponificacao.htm ,
Solicite à turma que criem um fórum para a comunidade escolar e discutam sobre como usar de forma consciente sabões e detergentes ou utilizar produtos descartáveis no cotidiano. Para desenvolver a atividade os alunos deverão acessar o
Link: http://www.forumeiros.com/
Os alunos poderão tornar disponível no fórum a charge abaixo e questionar: O que é melhor do ponto de vista da conservação do meio ambiente: utilizar sabões ou detergentes ou consumir produtos descartáveis no cotidiano?
Imagem disponível em: http://www.gazetadopovo.com.br/midia_tmp/600--EstacaoPUNKADA.jpg
Recursos Educacionais
| Nome | Tipo |
|---|---|
| Carboxylic-acid | Imagem |
| Ester | Imagem |
Recursos Complementares
Para conhecer a história do Sabão acesse o link: http://pt.wikipedia.org/wiki/Sab%C3%A3o
Para pesquisar: Como o sabão limpa? Link: http://www.brasilescola.com/quimica/como-sabao-limpa.htm
No link abaixo a turma poderá pesquisar sobre o conceito de Saponificação
Link: http://pt.wikipedia.org/wiki/Saponificação
Para conhecer as propriedades do sabão acesse o link:
Link: http://www.cdcc.sc.usp.br/quimica/experimentos/sabao.html
Neste site está disponível informação sobre como ocorre a Reação de Saponificação
Link: http://www.mundoeducacao.com.br/quimica/reacao-saponificacao.htm
Link: http://www.peretz.com.br/Professores/
Link: http://qnesc.sbq.org.br/online/qnesc02/exper2.pdf
Para conhecer a fórmula da reação de saponificação acesse o
Link: http://www.brasilescola.com/quimica/reacao-saponificacao.htm
Acesse o link abaixo para saber como transformar o óleo de cozinha usado em sabão.
Link: http://www.educador.brasilescola.com/estrategias-ensino/transformando-oleo-cozinha-usado-sabao.htm
Vídeo: http://www.youtube.com/watch?v=Onqjnf7SEJw
Livro: Civita, Victor. Enciclopédia do Estudante. Volume 8, Editora Abril Cultural, São Paulo, 1974.
Link: http://www.qmc.ufsc.br/qmcweb/artigos/bolhas_sabao.html
Aula: Produção de sabão - Link: http://portaldoprofessor.mec.gov.br/fichaTecnicaAula.html?aula=7701
Aula: De que é feito o sabão? - Link: http://portaldoprofessor.mec.gov.br/fichaTecnicaAula.html?aula=527
Avaliação
Para verificar a aprendizagem solicite aos alunos que se organizem em equipes, acessem os exercíicios disponíveis no link abaixo e resolvam as questões:
http://www.peretz.com.br/Professores/sejadmais05/exercicios/240505/exe-qui-3s-08.pdf
As atividades abaixo desenvolvidas ao longo das aulas poderão ser objeto de avaliação:
a) produção de um jornal contendo os conteúdos trabalhados nas aulas ou seja sobre saponificação; identificação das fórmulas estruturais e moleculares dos compostos químicos;
b) os questionamentos dirigidos ao professor
c) as contribuições com informações relativas as interações com parceiros da sala de aula;
d) a exploração e manuseio correto dos recursos tecnológicos;
e) a socialização de informações coletadas no desenvolvimento das atividades da Instrumentalização;
f) a elaboração dos textos de acordo com as regras da língua portuguesa.
Três estrelas 2 classificações
- Cinco estrelas 1/2 - 50%
- Quatro estrelas 0/2 - 0%
- Três estrelas 0/2 - 0%
- Duas estrelas 0/2 - 0%
- Uma estrela 1/2 - 50%
Denuncie opiniões ou materiais indevidos!
Opiniões
-
valeria mazucato, universidade federal de mato grosso do sul , Mato Grosso do Sul - disse:
valeriamazucato@hotmail.com02/05/2012
Cinco estrelasobrigada, gostei da forma como piropos a sequencia da aula e a clareza de idéias.
-
vagner, usuario , São Paulo - disse:
v.cezar@itelefonica.com.br02/01/2011
Uma estrelanão entendi nada pois eu só queria uma explicação lógica e objetiva do efeito em reação do alcool no sabão caseiro
- Sugestão de aula
- Aulas
- Coleções de aulas
- Criar aula
- Criar individual
- Criar em equipe
- Gerenciar equipes
- Minhas aulas
- Orientações
- Criando equipes
- Dicas para a produção de aulas
- Reflexões pedagógicas
- Utilizando a ferramenta
- Artigo: portal educacional
- Estatísticas de uso do Portal
- Estatísticas de aulas
- Estatísticas de recursos
- Estatísticas de visitas
- Recursos utilizados em aulas
- Reflexões pedagógicas
- Informações de cursos
- Cursos
- e-Proinfo
- Materiais de cursos
- Materiais de estudo
- Artigos e publicações
- Assuntos relevantes
- Avaliações
- Ciência do cotidiano
- Destaques internacionais
- Dicas práticas
- Educação profissional e tecnológica
- Entrevistas
- Estratégias pedagógicas
- Inovações tecnológicas
- Materiais de cursos
- Materiais de evento
- Orientações e diretrizes
- Parâmetros e referencias
- Programas em vídeos
- Tutoriais
- TVescola
- Ferramentas do portal
- Fórum
- Portal do Youtube
- Compartilhando apresentação
- Ferramentas pela internet
- Blog
- Compartilhe vídeos
- Comunicação on-line
- Crie e compartilhe apresentações
- Edite e compartilhe fotos
- Escrita colaborativa
- Junte-se a uma comunicade
- Lista de discussão
- Organize e compartilhe favoritos
- Podcast
- Rádio/TVs Universitárias e outros
- Redes Sociais
- Robô Ed
PLATAFORMA FREIRE
- Bibliotecas
- Capacitação Proinfo Integrado
- Cultura
- Dicionários, tradutores e enciclopédias
- Educação inclusiva
- Geoprocessamentos
- Inclusão digital
- Infográficos
- Jogos educativos
- Jornais
- Museus
- Observatórios e planetários
- Organizações governamentais
- Plataformas educacionais
- Portais educacionais e outros
- Portal MEC
- Prêmio professores do Brasil
- Produções de professores
- Projetos de escolas
- Projetos inovadores
- Projetos sociais e educacionais
- Rádio escola
- Recursos digitais
- Revistas
- Sites de busca
- Sites temáticos do portal e TVescola
- Softwares de edição e outros
- Softwares educacionais
- Um computador por aluno

- Ryan Oksenhorn
- Ryan Snow
- Sergio Caldara
- Shane Miler
- Shane Herzog
- Sotirios Papavasilopoulos
- Stephen JB Thomas
- Tarah
- Valera Nazarov
- ZbigniewMa K Flakus





 Carboxylic-acid
Carboxylic-acid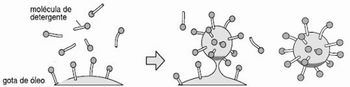
 Roupa suja se lava em casa
Roupa suja se lava em casa






